Elektrophoretische Verfahren – eine elektrochemische Analysemethode
Elektrochemische Analysemethoden beruhen auf physikalischen oder chemischen Vorgängen, die in elektrochemischen Zellen unter Ladungsaustausch an den Elektroden ablaufen. Sie werden meist zur quantitativen Analyse wässriger Lösungen genutzt.
Zu diesen Analysemethoden gehören u. a. Potenziometrie, Polarometrie, aber auch Konduktometrie und elektrophoretische Verfahren.
Bei allen Verfahren werden elektrische Größen z. B. die Zellspannung, Leitfähigkeit oder die Wanderungsgeschwindigkeit von Teilchen gemessen. Diese stehen in Zusammenhang mit der Art und der Konzentration der zu bestimmenden Substanz, die Analyt genannt wird. Die elektrische Messgröße kann entweder direkt oder im Rahmen einer Titration zur Äquivalenzpunktbestimmung herangezogen werden.
Die Elektrophorese gehört zu den elektrochemischen Analysemethoden. Sie ist ein analytisches Trennverfahren, das auf der Wanderung geladener Teilchen (Migration) in einer Elektrolytlösung unter Einwirkung eines elektrischen Feldes beruht. Die geladenen Teilchen können in gelöster oder in disperser Form vorliegen.
Durch den unterschiedlichen Aufbau der Teilchen, deren Ladung, Größe und Solvatation, ist die Kraftwirkung des elektrischen Feldes verschieden. Die Beweglichkeit bzw. Wanderungsgeschwindigkeit der Teilchen hängen daher hauptsächlich von ihrer Ladung, der auf sie einwirkenden Feldstärke und der Viskosität des Elektrolyten ab. Je höher die Ladung und je kleiner ein Teilchen ist, desto größer ist die Wanderungsgeschwindigkeit im elektrischen Feld.
Das Haupteinsatzgebiet dieser Methode ist die Biochemie zur Trennung und Charakterisierung von Aminosäuren, Peptiden und anderen Biomolekülen.
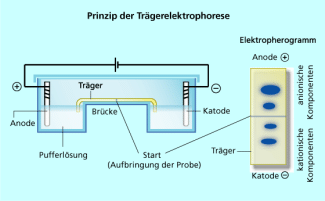
Prinzip der Trägerelektrophorese
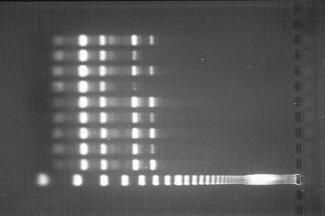
Aufgrund ihrer unterschiedlichen Beweglichkeiten lassen sich in Lösungen ionisch vorliegende bzw. ionisierbare Stoffe trennen. In der Praxis nutzt man dazu bevorzugt das Prinzip der Trägerelektrophorese. Das Trägermaterial z. B. Papier, Celluloseacetat oder ein gelartiges Material wird mit einer Pufferlösung getränkt und zwischen zwei Elektroden gebracht. Die Analyselösung wird an einer Startlinie aufgetragen und eine Gleichspannung im Bereich von 100 V und mehr angelegt, sodass die Ionen in der Lösung mit unterschiedlicher Geschwindigkeit zur entgegengesetzt geladenen Elektrode wandern. Nach Auftrennung des Gemisches kann man auf dem Trägermaterial die einzelnen Komponenten des Stoffgemisches mithilfe geeigneter Reagenzien sichtbar machen (Bild 1). Aus diesem Elektropherogramm kann man die Anzahl der Komponenten und nach vorheriger Kalibrierung auch ihre Art bestimmen.
-
Prinzip der Trägerelektrophorese
Gele als Trägermaterial
Als Trägermaterialien werden heute hauptsächlich gelartige Stoffe, z. B. Polyacrylamidgele oder Stärkegele eingesetzt. Deshalb spricht man auch von Gelelektrophorese.
Gele haben eine sehr hohe Viskosität, sodass sich hier die Größe und Gestalt der zu trennenden Teilchen viel stärker auswirkt als bei der klassischen Trägerelektrophorese.
Das Stoffgemisch, z. B. Proteine werden direkt auf das Gel aufgetragen. Nach Anlegen der Spannung wirkt das Gel wie ein molekulares Sieb, das die größeren Moleküle bzw. Ionen zurückhält und die kleineren passieren lässt (Bild 2). Auf diese Weise erfolgt die Trennung chemisch sehr ähnlicher Substanzen anhand ihrer Größe, also letztlich nach ihrer molaren Masse. Die Maschenweite des „molekularen Siebes“ kann man durch die Änderung der Konzentration des Polyacrylamids variieren.
Mit einem 30 %igen Gel trennt man Peptide mit bis zu 100 Aminosäureresten, mit einem 10 %igen Gel dagegen Proteine, die aus bis zu 1000 Aminosäureresten aufgebaut sind.
Unter den gleichen Analysebedingungen erhält man von einer bestimmten Probe immer wieder das gleiche charakteristische Elektropherogramm, einen „Fingerabdruck“ der Probe (Bild 3).
So beruht der in der Kriminaltechnik durchgeführte „ genetische Fingerabdruck “ zur Überführung von Straftätern auf der gelektrophoretischen Trennung von Nucleinsäuren.
Für die DNA-Analyse, Identitäts- und Reinheitsprüfungen von Arzneistoffen sowie umweltanalytische und medizinische Anwendungen ist die trägergebundene Elektrophorese von großer Bedeutung.
Anwendungen
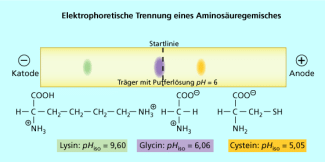
Besonders geeignet sind elektrophoretische Verfahren zur Trennung von Aminosäure- und Eiweißgemischen. Aminosäuren haben in wässrigen Lösungen eine zwitterionische Struktur. In Abhängigkeit von ihrem isoelektrischen Punkt liegen sie bei niedrigen pH-Werten hauptsächlich in kationischer und bei höheren pH-Werten hauptsächlich in anionischer Form vor.
Nach dem Prinzip der isoelektrischen Fokussierung kann so eine sehr scharfe Trennung der Komponenten erzielt werden. Dazu wird zwischen Anode und Katode zusätzlich ein pH-Gradient gelegt. Die Komponenten wandern dann nur bis zu der Stelle, wo der pH-Wert im Gradientenfeld dem isoelektrischen Punkt entspricht.
Die Kapillarelektrophorese ist eine Weiterentwicklung der klassischen Trägerelektrophorese. Hier erfolgt die Trennung von kleinsten Substanzmengen in einer dünnen Quarzglaskapillare. Das hochmoderne Verfahren kann computergestützt und vollautomatisch durchgeführt werden. Die Kapillarelektrophorese wird auch zur Trennung anorganischer Ionen eingesetzt.
-
Elektrophoretische Trennung eines Aminosäuregemisches
-
Gelelektropherogramm