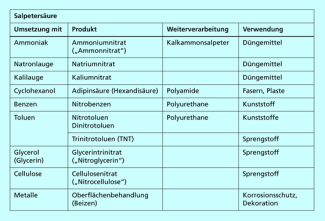
Verwendung von Salpetersäure
Salpetersäure ist eine der drei wichtigste Säuren in der chemischen Industrie. Sie wird hauptsächlich zur Herstellung von Stickstoffdüngemitteln verwendet. Außerdem dient sie als Ausgangsstoff für die Synthese von Sprengstoffen, Kunststoffen und Chemiefasern, und sie wird zum Beizen von Metallen eingesetzt.
Der größte Teil der Salpetersäure, 60-80 %, wird zur Herstellung von Stickstoffdüngemitteln verwendet.
Wichtige Düngemittel auf der Basis von Salpetersäure sind Ammoniumnitrat und Kalkammonsalpeter. Ersteres ist thermisch instabil und kann bei über 300 °C explosionsartig zu Distickstoffmonooxid und Wasser zerfallen, weshalb es in der BRD als Düngemittel verboten ist. Im Kalkammonsalpeter, einem häufig verwendeten Dünger, ist dem Ammoniumnitrat Kalk beigemischt, wodurch die Explosion verhindert wird. Außerdem wird durch den Kalk die im Boden frei werdende Säure neutralisiert und dadurch der Versauerung des Bodens entgegenwirkt.
-
Kalkammonsalpeter ist ein wichtiges Stickstoffdüngemittel.

![]()
Etwa 5-10 % der Salpetersäure werden in der organischen Chemie für Oxidationsreaktionen eingesetzt. Die dabei erhaltenen Verbindungen dienen hauptsächlich der Produktion von Polymerwerkstoffen, so wird z. B. Adipinsäure (Hexandisäure), ein wichtiger Ausgangsstoff für die Herstellung von Polyamiden wie Nylon und Perlon, durch oxidative Spaltung von Cyclohexan mit Salpetersäure als Oxidationsmittel synthetisiert.
Weitere 5-10 % dienen für Nitrierungsreaktionen. Wichtige Nitroverbindungen sind z. B. der bekannte Sprengstoff Trinitrotoluen (TNT), manche Naphthol-Farbstoffe (z. B. Naphtholgelb S) und außerdem Pharmazeutika, z B. das Antibiotikum Chloramphenicol oder manche Chemotherapeutika.
![]()
Dinitrotoluen wird in großen Mengen als wichtiges Zwischenprodukt für die Synthese von Polyurethanen hergestellt.
Unter Verwendung von Salpetersäure werden auch die Sprengstoffe Nitrocellulose und Nitroglycerin hergestellt, deren richtige Namen Cellulosenitrat und Glyceroltrinitrat lauten, denn sie sind keine Nitroverbindungen, sondern Ester der Salpetersäure.
![]()
Ein weiteres Anwendungsgebiet von Salpetersäure ist die Oberflächenbehandlung von Metallen, d. h. das Beizen oder Ätzen z. B. von rostfreiem Stahl.
Die Salze der Salpetersäure, die Nitrate, werden als Sprengstoffe oder in Feuerwerkskörpern verwendet. Der erste bekannte Sprengstoff, das Schwarzpulver, ist eine Mischung aus 75 % Kaliumnitrat, 10 % Schwefel und 15 % Holzkohlepulver.
-
Verwendung von Salpetersäure