Aldehyde und Ketone
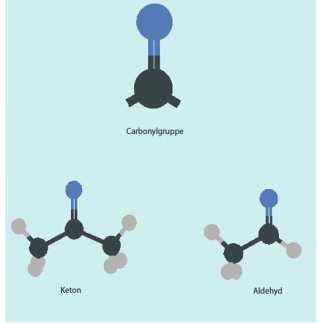
Aldehyde und Ketone sind wichtige Verbindungsklassen der organischen Chemie. Die wichtigsten Vertreter sind die Alkanale und Alkanone. Als funktionelle Gruppe enthalten die Moleküle beider Stoffklassen die Carbonylgruppe (-C=O).
Aldehyde und Ketone zeichen sich u. a. durch intensive Grüche aus. Sie finden deshalb Anwendung als Geruchs- und Aromastoffe. Sowohl Aldehyde als auch Ketone lassen sich zu Alkoholen reduzieren. Im Gegensatz dazu lassen sich nur Aldehyde leicht oxidieren, wobei Carbonsäuren entstehen.
Aldehyde und Ketone sind einander ähnliche Verbindungsklassen, die dementsprechend ähnliche chemische und physikalische Eigenschaften aufweisen. Sie lassen sich z. B. gut reduzieren, sind meist leicht flüchtig, brennbar und besitzen oft einen charakteristischen, intensiven Geruch. Allerdings gibt es auch Unterschiede, so lassen sich Ketone im Gegensatz zu den Aldehyden nicht oxidieren.
Die Gemeinsamkeiten der beiden Substanzklassen, lassen sich durch die Ähnlichkeit der funktionellen Gruppen der Aldehyde und der Ketone erklären. Beiden gemein ist die -C=O-Gruppe, die auch Carbonyl-Gruppe genannt wird. In dieser funktionellen Gruppe ist das vierwertige (tetravalente) Kohlenstoffatom, auch Carbonyl-Kohlenstoffatom genannt, über eine Doppelbindung mit einem Sauerstoffatom verbunden. Die beiden restlichen Bindungsmöglichkeiten (Valenzen) können mit Kohlenstoff- oder Wasserstoffatomen besetzt werden. Genau darin unterscheiden sich Aldehyde und Ketone (siehe Bild 1).
In Aldehyden ist immer (mindestens) eine der beiden Bindungsmöglichkeiten (Valenzen) mit einem Wasserstoffatom besetzt. Die funktionelle Gruppe der Aldehyde (Aldehyd-Gruppe) ist also:
![]()
Die verbleibende freie Valenz (Bindungsmöglichkeit) kann einen beliebigen Kohlenwasserstoffrest tragen. Stammt der Rest von den Alkanen ab, dann bezeichnet man das entsprechende Aldehyd auch als Alkanal. Dabei steht die Endung -al für die Aldehydgruppe. Der systematische Name ergibt sich dann aus der Bezeichnung des Kohlenwasserstoffes mit der Endung -al. Ausserdem sind häufig "Trivialnamen" im Gebrauch.
| Formel | Nomenklatur | "Trivialname" |
| Methanal | Formaldehyd | |
Ethanal | Acetaldehyd | |
| Butanal | Butyraldehyd |
In Ketonen sind beide freien Valenzen des Carbonyl-Kohlenstoffatoms mit beliebigen Kohlenwasserstoffresten besetzt. Sind die beiden Kohlenwasserstoffreste indentisch, spricht man auch von symmetrischen Ketonen, sind sie verschieden, von unsymmetrischen (oder asymmetrischen) Ketonen. Die funktionelle Gruppe wird als Keto-Gruppe bezeichnet, darunter versteht man eine Carbonylgruppe die zwei Kohlenwasserstoffreste trägt.
![]()
Die Endung -on zeigt das Vorhandensein der Ketogruppe an. Der vollständige Name ergibt sich aus der Bezeichnung für das Kohlenwasserstoffgrundgerüst und der Endung -on. Zur genauen Bezeichnung ist es noch notwendig die Position der Ketogruppe anzugeben. Dies geschieht durch Einfügen einer Zahl vor der Endung -on, welche die Position angibt. Dabei beginnt man die Nummerierung der Kohlenstoffatome von der kürzeren Seite aus, so dass möglichst niedrige Zahlen benötigt werden. Auch bei Ketonen werden oftmals nichtsystematische Namen verwendet, wobei meist die beiden Seiten der Ketogruppe einzeln benannt werden.
| Formel | Name | alternative Bezeichnungen |
| Propan-2-on | Dimethylketon / Aceton | |
| Butan-2-on | Ethyl-Methyl-Keton | |
| Hexan-3-on | Ethyl-Propyl-Keton |
Reaktionen von Aldehyden und Ketonen
Aldehyde und Ketone lassen sich von vielen Reduktionsmitteln reduzieren. Dabei entstehen als Reaktionsprodukte die entsprechenden Alkohole. Da die Aldehydgruppe immer endständig ist, entstehen aus Aldehyden durch Reduktion immer primäre Alkohole. Aus Ketonen entstehen dagegen immer sekundäre Alkohole. Aldehyde und Ketone lassen sich auch durch Umkehrung dieser Reaktion, also durch die Oxidation von primären bzw. sekundären Alkoholen, herstellen.
![]()
Da die Aldehyde im Gegensatz zu den Ketonen am Carbonyl-Kohlenstoffatom noch ein Wasserstoffatom tragen, lassen sich Aldehyde leicht weiter oxidieren. Das Produkt der Oxidation ist dann eine Carbonsäure. Aldehyde wirken also, im Gegensatz zu Ketonen, reduzierend.
![]()
Diese Eigenschaft kann man auch für Nachweisreaktion von Aldehyden ausnutzen. So reduzieren beispielsweise Aldehyde die Kupfer(II)-Ionen in fehlingscher Lösung zu Kupfer(I), was man an der Fällung eines roten Kupfer(I)-oxid-Niederschlages erkennen kann.
-
Aldehyde und Ketone enthalten die Carbonylgruppe
Bedeutung von Aldehyden und Ketonen
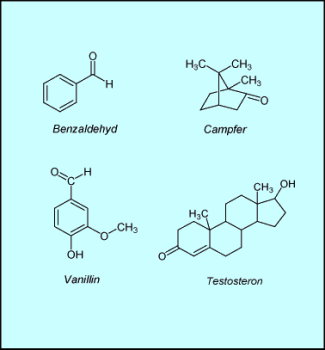
Da Aldehyde und Ketone meist intensive Gerüche besitzen werden sie u. a. als Duft- oder Aromastoffe verwendet. Benzaldehyd z. B. ist der einfachste aromatische Aldehyd. Er ist eine farblose ölige Flüssigkeit, die nach bitteren Mandeln riecht. Benzaldehyd wird in der Lebensmittelindustrie als Zusatzstoff (Bittermandelaroma) eingesetzt. Auch Vanillin z. B. enthält eine Aldehydgruppe.
Viele Botenstoffe im menschlichen Körper sind Ketone, z. B. das männliche Sexualhormon Testosteron. Auch in Pflanzen gibt es viele Ketone, wie z. B. der Campher. Man verwendet ihn für Salben die die Durchblutung der Haut fördern.
Eine ganz besondere Rolle spielen die Kohlenhydrate (Zucker). Neben den Hydroxylgruppen enthalten die Zucker auch die Carbonylgruppe als funktionelle Gruppe. Zucker können sowohl Aldehyde als auch Ketone sein. Dementsprechend unterteilt man sie auch in Ketosen (mit Ketogruppe) und Aldosen (mit Aldehydgruppe). Im Gegensatz zu den Ketosen wirken die Aldosen reduzierend und werden deshalb auch als reduzierende Zucker bezeichnet.
![]()
-
Beispiele für Aldehyde und Ketone