Das aromatische System
Aromatische Verbindungen sind cyclische Verbindungen, deren Ringatome hybridisiert sind. Somit liegen die Ringatome in einer Ebene. Das an jedem Atom des Rings verbleibende p-Orbital steht ober- und unterhalb dieser Ebene. Die Elektronen im gebildeten System sind delokalisiert, was zu einer Energieabsenkung (Mesomerieenergie) führt. Die Anzahl der Elektronen im System entspricht der Hückel-Regel.
Aromaten
Aromatische Verbindungen sind grundsätzlich cyclische Verbindungen, die folgende Kriterien erfüllen:
- Alle Atome des Ringes sind hybridisiert und liegen somit in einer Ebene.
- Die mit einem Elektron besetzten p-Orbitale stehen senkrecht oberhalb und unterhalb dieser Ebene.
- Die Anzahl der Elektronen in diesen p-Orbitalen muss der Hückel-Regel, entsprechen und beträgt 4n+2 (n ist eine positive natürliche ganze Zahl).
- Die Elektronen in den Orbitalen sind in einem p-System delokalisiert. Sie sind über den gesamten Ring verteilt, was zu einer Energieabsenkung der Mesomerieenergie oder Resonanzenergie führt.
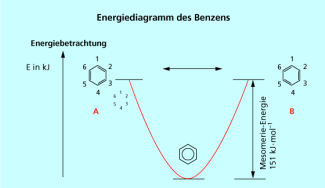
Erfüllt eine cyclische Verbindung die vier Kriterien, hat sie einen aromatischen Zustand. Die Delokalisierung des Elektronensystems führt immer zu einer Energieabsenkung und somit zu einer Stabilisierung der Verbindung (Bild 2).
Einteilung der aromatischen Verbindungen
Die Einteilung der aromatischen Verbindungen kann in zwei Hauptgruppen erfolgen:
- Bei den aromatischen Kohlenwasserstoffen sind im Ring nur Kohlenstoffatome miteinander verbunden.
- Die Heteroaromaten enthalten außerdem mindestens ein anderes Atom.
Beide Hauptgruppen werden noch einmal in monocyclische und kondensierte Aromaten/Heteroaromaten (Heterocyclen) unterteilt.
![]()
-
Energiediagramm von Benzen
Die Unterscheidung zwischen Aromat und Cycloalken
Für die Entscheidung, ob eine entsprechende Verbindung aromatisch ist, müssen alle Kriterien überprüft werden. So kann beispielsweise das Cyclooctatetraen (Bild 3) nicht planar sein. Die Innenwinkelsumme in einem regulären 8-Eck beträgt 1080 °. Daraus folgt, dass alle C-C-C-Bindungswinkel 135 ° hätten. Bei Kohlenstoffatomen ist aber der Bindungswinkel 120 °. Deshalb liegt das Cyclooctatetraen in einer Wannenstruktur vor.
Ein 5-gliedriger Kohlenwasserstoff, wie das Cyclopentadien (Bild 4), kann ebenfalls nie aromatisch sein. Ein Kohlenstoffatom muss als Kohlenstoffatom vorliegen. Der Bindungswinkel beträgt 109,5 °, das heißt, dieses Atom steht außerhalb der Ebene, die die vier Kohlenstoffatome bilden. Außerdem enthält das System nur 4 Elektronen. Das widerspricht der Hückel-Regel.
Im Gegensatz dazu sind 5-gliedrige Heterocylen, wie das Pyrrol (Bild 5) aromatisch, da ein freies ungebundenes Elektronenpaar des Heteroatoms in das Elektronensystem einbezogen wird.
![]()

