Herstellung von Methanol
Methanol ist nach seinen Verwendungsmöglichkeiten und der produzierten Menge der wichtigste Alkohol. Methanol wird durch Reaktion von Kohlenstoffmonooxid und Wasserstoff in einem Reaktor hergestellt.
Bedeutung von Methanol
Methanol ist nach seinen Verwendungsmöglichkeiten und der produzierten Menge der wichtigste Alkohol. Pro Jahr werden weltweit insgesamt mehr als 20 Mio. Tonnen Methanol hergestellt.
Das Alkanol wird für die Herstellung verschiedenster organischer Stoffe, z. B. Formaldehyd, Essigsäure oder Kunststoffe benötigt. Auch als Lösungsmittel für Lacke und Farben und als Vergaserkraftstoff oder Kraftstoffzusatz kann Methanol eingesetzt werden.
Methanol wird in einer Gleichgewichtsreaktion aus Synthesegas in einem Reaktor hergestellt.
Ausgangsstoffe: Synthesegas (aus Erdöl, Erdgas oder Kohle) mit Kohlenstoffmonooxid und Wasserstoff
Reaktionsprodukt: Methanol
Chemische Reaktion:
; Q = -92 kJ/mol
Ablauf der Methanolsynthese
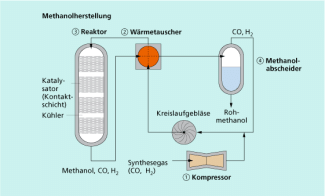
Kompressor: Verdichten des Synthesegases (aus Kohlenstoffmonooxid und Wasserstoff) auf 5-35 MPa
Wärmeaustauscher: Erhitzen des Gasgemisches auf 250-350 °C
Reaktor: Entstehung von Methanol durch Kontakt mit dem Katalysator (verschiedene Kupfer-, Aluminium- und Zink-Oxide). Der Umsatz beträgt bei einmaligem Durchgang durch den Reaktor je nach Druck und Temperatur 20-50 %.
Abtrennung des Rohmethanols:
- Abkühlung des Reaktionsgemisches und Kondensation des Rohmethanols
- Abtrennung von den nicht umgesetzten Ausgangsstoffen, die dann in den Kreislauf zurückgeführt werden
- Reinigung des Rohmethanols durch Destillation
-
Methanolherstellung