Energie
Energie ist die Fähigkeit, mechanische Arbeit zu verrichten, Wärme abzugeben oder Licht auszustrahlen.
- Formelzeichen: E
- Einheit: ein Joule (1 J)
Die Energie ist eine Zustandsgröße und in abgeschlossenen Systemen eine Erhaltungsgröße.
Energie ist überall in Natur und Technik vorhanden. Menschen, Tiere und Pflanzen benötigen sie für ihre Entwicklung.
Technische Geräte wie Radios, Kühlschränke, Fernsehgeräte oder Computer brauchen zum Betrieb Energie. Ohne Energie würde kein Zug fahren und kein Flugzeug fliegen. Trotzdem kann man Energie zumeist nicht sehen, fühlen oder anfassen. Man kann sie aber an ihren Wirkungen erkennen. Allgemein gilt in den Naturwissenschaften für die Größe Energie:
Energie ist die Fähigkeit, mechanische Arbeit zu verrichten, Wärme abzugeben oder Licht auszustrahlen.
Benannt ist die Einheit der Energie nach dem englischen Physiker JAMES PRESCOTT JOULE (1818 - 1889).
Vielfache der Einheit ein Joule (1 J) sind ein Kilojoule (1 kJ), ein Megajoule (1 MJ) und ein Gigajoule (1 GJ):
- 1 kJ = 1000 J
- 1 MJ = 1000 kJ = 1000000 J
- 1 GJ = 1000 MJ = 1000000 kJ = 1000000000 J
- ein Newtonmeter (1 Nm): 1 Nm = 1J
eine Wattsekunde (1 Ws): 1 Ws = 1 J
eine Steinkohleneinheit (1 SKE): 1 SKE = 29,3 MJ (Das ist der durchschnittliche Energieinhalt von 1 kg Steinkohle, der bei vollständiger Verbrennung frei wird.)
eine Rohöleinheit (1 RÖE): 1 RÖE = 41,9 MJ (Das ist der durchschnittliche Energieinhalt von 1 l Rohöl, der bei vollständiger Verbrennung frei wird.)Energie als Zustands- und Erhaltungsgröße
Die Größe Energie kennzeichnet den Zustand eines Körpers, eines elektrischen Feldes oder eines magnetischen Feldes. Man bezeichnet in der Physik eine solche Größen als Zustandsgröße im Unterschied zu einer Prozessgröße, die einen Vorgang charakterisiert.
Für einen abgeschlossenen Bereich oder für ein abgeschlossenes System bleibt die Gesamtenergie immer erhalten. Die Energie ist somit auch eine Erhaltungsgröße, für die ein Erhaltungssatz – der Energieerhaltungssatz – gilt.
Energieformen und Energieträger
Energie kann in unterschiedlichen Formen auftreten, z. B. in Form von elektrischer, thermischer, mechanischer oder chemischer Energie oder als Energie elektrischer und magnetischer Felder Lichtenergie, elektrische Energie, magnetische Energie). Darüber hinaus gibt es die Energieformen Kernenergie, potenzielle Energie und kinetische Energie.
Körper oder Raumbereiche, die Energie besitzen, bezeichnet man als Energieträger oder Energiequellen.
-
Energie im Überblick
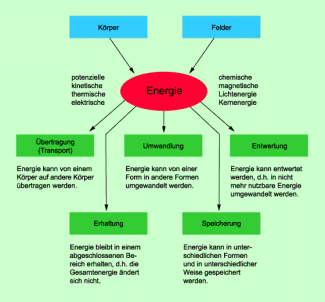
Energie im Wandel
In einem abgeschlossenen Bereich (abgeschlossenen System) bleibt die Gesamtenergie stets gleich groß, aber:
- Energie kann von einem Körper auf andere Körper übertragen (transportiert) werden,
- Energie kann von einer Form in andere Formen umgewandelt werden,
- Energie kann entwertet werden, d. h. in solche Formen umgewandelt werden, die für den Menschen schlecht nutzbar sind,
- Energie kann gespeichert werden.

