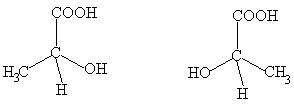Formen der Isomerie in organischen Verbindungen
Unerklärlich scheint es auf den ersten Blick, dass Stoffe mit der gleichen Anzahl und Art von Atomen, mit gleicher Summenformel, aber unterschiedlicher Anordnung dieser Atome so verschieden sein sollen. Solche Verbindungen werden Isomere genannt. Sie weisen nicht nur unterschiedliche physikalische Eigenschaften auf, sondern reagieren auch unterschiedlich und haben unterschiedliche Bedeutsamkeit in der Biochemie.
Entwicklung des Begriffs
Der Wissenschaftler JUNGIUS soll im 19. Jahrhundert die ersten Überlegungen zur Isomerie angestellt haben. Der Begriff bedeutet soviel wie „gleiche Teile“.
JUSTUS VON LIEBIG (1803-1873) beschäftigte sich mit der Elementaranalyse von organischen Stoffen und schaffte es, dass sie zur Routineuntersuchung wurde. Dabei stellte er 1823 fest, dass einige Stoffe gleiche Summenformeln aufweisen. So z. B. die Cyansäure (HOCN) und die Knallsäure (HCNO). Diese beiden Verbindungen haben aber trotz gleicher Summenformel unterschiedliche chemische Eigenschaften. LIEBIG formulierte zur Veranschaulichung, dass aus gleichen Buchstaben ebenfalls unterschiedliche Worte gebildet werden können: „Dome – Mode – Odem“.
FRIEDRICH WÖHLER (1800-1882) stellte 1828 aus Ammoniumcyanat Harnstoff her und synthetisierte damit eine organische Verbindung aus einer anorganischen. Dass Harnstoff und Ammoniumcyanat die gleiche Summenformel besitzen, also isomer sind, stellte er erst später fest.
Die Begriffe Isomerie und Isomere wurde 1830 von JÖNS JACOB BERZELIUS (1779-1848) in die Chemie eingeführt. Nach BERZELIUS sind isomere Stoffe die, „die gleiche Elementaratome, aber in ungleicher Weise zusammengelegt“ enthalten.
Der Begriff Isomerie
Isomere Verbindungen sind Verbindungen mit gleicher Summenformel, also gleicher atomarer Zusammensetzung, aber unterschiedlicher Struktur. Dadurch ergeben sich unterschiedliche Eigenschaften der Verbindungen (z. B. Geruch, Siede- und Schmelztemperatur, chemische Reaktionsfähigkeit).
In der organischen Chemie haben Isomere die gleiche Summenformel (Bruttoformel), aber unterschiedliche Strukturformeln. Auch die Benennung der Stoffe ist unterschiedlich.
Es gibt verschiedene Möglichkeiten für Isomerien.
![]()
Konstitutionsisomere
Konstitutionsisomere sind Verbindungen mit gleicher Summenformel, aber einer unterschiedlichen Verknüpfung von Atomgruppen oder Atomen im Molekül.
Die einfachste Form der Bildung von Isomeren ist durch Verzweigung der Kohlenstoffketten. Die Zahl der möglichen Isomere mit einer Summenformel wächst mit der Zahl der Atome rasch an. Am Beispiel der Alkane wird dies deutlich. Methan, Ethan und Propan besitzen keine Isomere, Butan zwei.
Pentan ( ) besitzt drei Isomere, Hexan ( ) hat nicht vier, sondern fünf, Heptan ( ) besitzt schon neun verschiedene Konstitutionsisomere, und die Anzahl der möglichen isomeren Verbindungen wächst rasch an, z. B. bei dem Alkan
- mit 15 Kohlenstoffatomen auf 4 347 Isomere,
- mit 25 Kohlenstoffatomen auf 36 797 588 Isomere,
- und mit 40 Kohlenstoffatomen gar auf 62 491 178 805 831 Isomere.
Grundsätzlich gilt, dass verzweigte Verbindungen niedrigere Schmelz- und Siedetemperaturen aufweisen als unverzweigte. Das hängt vor allem mit der kleineren Oberfläche und den daraus resultierenden geringeren van-der-Waals-Kräften zusammen.
Eine andere Form der Konstitutionsisomerie besteht darin, dass beispielsweise funktionelle Gruppen im Molekül anders angeordnet sind.
Beispiel:
Propan-1-ol: Schmelztemperatur -126,2 °C, Siedetemperatur 97,2 °C
Propan-2-ol: Schmelztemperatur -88,5 °C, Siedetemperatur 82,3 °C
Strukturformel von n-Butan
Auch die Isomeren bei mehrfach substituierten Aromaten sind Konstitutionsisomere. Sie werden aber häufig als Stellungsisomere bezeichnet.
![]()
Außerdem gibt es auch die Möglichkeit, dass sich Mehrfachbindungen an unterschiedlichen Stellen im Molekül befinden.
Beispiel:
![]()
![]()
Stereoisomere
Stereoisomere sind Moleküle mit gleicher Konstitution, aber einer unterschiedlichen räumlichen Anordnung der Atome.
Es gibt unterschiedliche Formen der Stereoisomerie. Ein Beispiel ist die optische Isomerie. Zwei Moleküle sind einander spiegelbildlich, die räumliche Lage der Atome ist bei gleicher Verknüpfung also verschieden.
Beispiel: Milchsäure
![]()
Milchsäure kann in einer L-Form (diese dreht polarisiertes Licht nach links) und in einer spiegelbildlich gleichen D-Form (diese dreht polarisiertes Licht nach rechts) vorkommen.
Verblüffend ist die unterschiedliche pharmakologische, toxische oder stoffwechselaktive Wirkung, die besonders bei den spiegelbildlichen Isomeren (Stereoisomeren) zu beobachten ist.
Alle auf der Erde lebenden Lebewesen bestehen nur aus L-Aminosäuren und können auch nur L-Formen von organischen Verbindungen verstoffwechseln. Diese seltsame Eigenschaft ist bis heute unerklärlich. Auch bei Arzneistoffen sind oft nur bestimmte Isomere wirksam.
-
Butanol bildet vier Isomere aus.
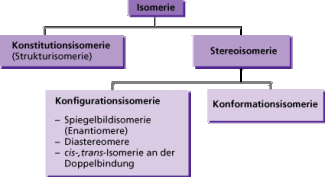
Konfigurationsisomerie
Befindet sich in einem Molekül ein Kohlenstoffatom mit vier unter-schiedlichen Substituenten (asymmetrisches Kohlenstoffatom), können Bild und Spiegelbild nicht zur Deckung gebracht werden. Solche Verbindungen, die zwei Spiegelbildisomere bzw. Enantiomere besitzen, nennt man chirale Verbindungen.
Die cis-, trans-Isomerie ist eine Form der Konfigurationsisomerie, die auftritt, wenn an beiden Enden der C=C-Doppelbindung je zwei verschiedene Substituenten gebunden sind. Die größeren Substituenten können entgegengesetzt, trans-, oder auf einer Seite der Doppelbindung, cis-, angeordnet sein.
![]()
D-, L-Nomenklatur, FISCHER-Projektion
Die FISCHER-Projektion ist die Darstellung der räumlichen Struktur tetraedrisch koordinierter Kohlenstoffatome in der Ebene. Chirale Verbindungen können so eindeutig als D- oder L-Enantiomer identifiziert werden. Folgende Regeln wurden von EMIL FISCHER am Glycerinaldehyd als Stammverbindung für die FISCHER-Projektion aufgestellt:
| – | Die längste Kohlenstoffkette steht vertikal, das am höchsten oxidierte Kohlenstoffatom steht oben und trägt die Nummer 1. |
| – | Die beiden horizontalen Bindungen am betrachteten Kohlenstoffatom zeigen aus der Papierebene auf den Betrachter zu, die beiden vertikalen in die Papierebene. |
| – | Steht die OH-Gruppe am chiralen Kohlenstoffatom rechts, gehört das Molekül in die D-Reihe – steht sie links, gehört es in die L-Reihe. |
R-, S-Nomenklatur
Mit der FISCHER-Nomenklatur wird nur die absolute Konfiguration eines Kohlenstoffatoms eindeutig festgelegt. Die Festlegung der absoluten Konfiguration nach CAHN, INGOLD und PRELOG ermöglicht die Zuordnung für alle Chiralitätszentren in einem Molekül. Dabei werden den Substituenten am asymmetrischen C-Atom Prioritäten zugeordnet (Regeln). Blickt man jetzt auf das Kohlenstoffatom in Richtung des Substituenten mit der kleinsten Priorität, ordnen sich die anderen im (R) oder gegen den Uhrzeigersinn (S) an.
-
Chiralität heißt „Händigkeit“. Der Begriff erklärt sich dadurch, dass die rechte und die linke Hand Spiegelbildisomere sind. Der optische Drehwert gibt an, wie polarisiertes Licht beim Durchstrahlen der Probe aus der Ebene gedreht wird.

Konformationsisomere
Konformationsisomere sind Isomere, die durch Rotationen um die C-C-Einfachbindung entstehen.
Sie sind normalerweise nicht zu unterscheiden, da diese Rotation ständig und mit hoher Geschwindigkeit stattfindet. Betrachtet wird die Stellung von je einem Substituenten an zwei benachbarten C-Atomen. Sind die Substituenten sehr groß, wird die Rotation behindert, sodass einzelne Zustände experimentell nachweisbar sind.
Zu den Konformationsisomeren zählt man aber auch die einzelnen Zustände des Cyclohexanrings, die durch das sogenannte Durchschwingen entstehen (Sessel – Wanne – Sessel). Zu beachten ist dabei, dass bei diesem „Durchschwingen“ äquatoriale (e) und axiale (a) Substituenten die Plätze tauschen.
Konformationsisomere lassen sich auch anschaulich in der Sägebockschreibweise darstellen:
gestaffelt, anti | verdeckt (eclipsed) |
-
Konformationsisomerie