Die Brennstoffzelle – umweltfreundliche Kraftpakete
Die Brennstoffzelle ist ein Spezialfall eines galvanischen Elements, bei dem chemische Energie direkt in elektrische Energie umgewandelt wird. Während sich bei Batterien und Akkumulatoren die an den chemischen Reaktionen beteiligten Materialien allmählich verbrauchen, werden bei der Brennstoffzelle die Ausgangsstoffe und Produkte der Reaktion kontinuierlich zu- und abgeführt. Betrieben wird sie häufig mit Wasserstoff und Sauerstoff. Anstelle von Wasserstoff können aber auch andere Brennstoffe genutzt werden. Ein einzelnes Element einer Wasserstoff-Brennstoffzelle liefert eine Gleichspannung von knapp einem Volt. Praktische Ausführungen arbeiten mit Hintereinanderschaltungen vieler solcher Elemente.
Das grundlegende Prinzip wurde bereits 1839 entdeckt. Intensive Forschungen zur technischen Nutzung begannen aber erst ab etwa 1960. Gegenwärtig ist die Entwicklung leistungsfähiger Brennstoffzellen ein Schwerpunkt der technischen Forschung.
Umweltfreundliche Kraftpakete
Der Treibstoffbedarf der Menschheit ist riesengroß und kann nur noch einige Jahre durch Erdöl und Co. gedeckt werden. Die Verbrennung fossiler Energieträger verstärkt zudem den Treibhauseffekt, sodass es auch aus umweltchemischen Gründen dringend geboten ist, nach alternativen Energiequellen zu suchen.
Ein umweltfreundlicher Energieträger scheint fotovoltaisch erzeugter Wasserstoff zu sein, bei dessen Verbrennung Energie frei wird, ohne dass dabei Kohlenstoffdioxid entsteht. Unkontrolliert reagiert Wasserstoff jedoch explosionsartig mit Sauerstoff (Knallgasreaktion), sodass frei werdende Energie erst mithilfe innovativer Technologien nutzbar gemacht werden muss. Ein solches Verfahren, in das Forscher und besonders Autobauer große Hoffnungen setzen, ist die sogenannte „kalte Verbrennung“ von Wasserstoff in Brennzellen. Dabei wird die chemische Energie des Brennstoffs in elektrische Energie umgewandelt und kann für verschiedenste Zwecke genutzt werden. Brennstoffzellen sind galvanische Zellen, in denen Wasserstoff und Sauerstoff kontrolliert zur Reaktion gebracht werden. Unter kontinuierlicher Zufuhr der Edukte wird chemische Energie bedarfsgerecht in elektrische Energie umgewandelt. Sie können daher im Gegensatz zu Batterien, deren Nutzungsdauer begrenzt ist, theoretisch unbegrenzt betrieben werden.
Funktionsprinzip und Arten von Brennstoffzellen
Das Prinzip der Brennstoffzelle ist älter als man denkt: Bereits 1839 baute Sir WILLIAM GROVE (1811-1896) eine einfache galvanische Zelle mit Platinelektroden in Schwefelsäure. Wenn er diese getrennten Elektroden mit Wasserstoff bzw. Sauerstoff umspülte, konnte er eine Spannung von etwa einem Volt messen. Die von Grove galvanische Gasbatterie genannte Erfindung geriet jedoch bald in Vergessenheit, weil es ihm nicht gelang, daraus eine alltagstaugliche Energiequelle zu entwickeln. Mit dem damaligen Stand der Technik konnte er u. a. die Sicherheitsprobleme bei der Handhabung von Wasserstoff und Sauerstoff (Knallgasbildung) nicht zufiedenstellend lösen. Zudem erwiesen sich seine Platinelektroden als nicht leistungsfähig genug.
Trotzdem funktionieren moderne Brennstoffzellen noch heute nach dem von Grove entdeckten Grundprinzip: Wasserstoff und Sauerstoff werden elektrochemisch an getrennten Elektroden zur Reaktion gebracht. Die Gesamtreaktion der galvanischen Zelle entspricht der Knallgasreaktion. Dabei wird die chemische Energie des Wasserstoffs und des Sauerstoffs kontrolliert in elektrische Energie umgewandelt.
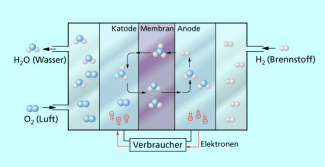
In modernen Brennstoffzellen trennt eine ionendurchlässige Polymermembran die Elektrodenräume. Diese Membran ist ca. 0,1 mm dick und muss gasdicht sein, damit Sauerstoff und Wasserstoff nicht direkt miteinander reagieren. Sie ist durchlässig für Oxonium-Ionen bzw. Protonen, jedoch undurchlässig für Elektronen. Die Elektroden müssen gegen den Elektrolyten beständig sein und einen hohen elektrochemischen Stoffumsatz gewährleisten. Dazu werden spezielle Kohlenstoff- bzw. Metallplatten mit katalytisch aktivem Palladium bzw. einer Platinlegierung beschichtet. Unter dem Einfluss des Katalysators entstehen an der Anode Oxonium-Ionen. Sie wandern durch die Membran, während die Elektronen über einen Verbraucher zur Katode geführt werden. Dort werden sie von Sauerstoffatomen aufgenommen, die mit den Oxonium-Ionen zu Wassermolekülen reagieren.
Die Wassermenge, die als Oxonium-Ionen aus dem Katodenraum in den Anodenraum eingetragen wurde, wird wieder zur Katode zur Konstanthaltung des Füllstands zurückgeführt. Der Rest wird aus der Zelle abgeführt und kann genutzt werden.
Auf diese Weise erreichen Polymerelektrolyt-Brennstoffzellen (PEMFC) eine Ausgangsleistung von bis zu 500 W, wenn entsprechend viele Elemente zu einem Stapel (engl.: stack) zusammengeschaltet werden. Die PEMFC eignen sich besonders zum Antrieb von Pkws mit Elektromotoren und als Energiewandler in Brennstoffzellen-Heizgeräten, die Einfamilienhäuser mit Strom und Wärme versorgen. Für weitere Anwendungen wurden verschiedene Typen von Brennstoffzellen entwickelt, die teilweise andere Brennstoffe und andere Elektrolyte nutzen. Sie unterscheiden sich deshalb in der Betriebstemperatur und der Ausgangsleistung.
Vor allem mit Festoxidbrennstoffzellen (SOFC) lassen sich noch höhere Leistungen erzielen als mit den PEMFC. Aufgrund ihrer hohen Betriebstemperatur (> 500 °C) können sie mit Erdgas betrieben werden. Die Abwärme wird ins Fernwärmenetz eingespeist, sodass Brennstoffzellen-Heizkraftwerke einen Gesamtwirkungsgrad von über 90 % erreichen.
Brennstoffbereitstellung – Wasserstoffwirtschaft
Die Vorteile der Brennstoffzelle, die Vermeidung von Kohlenstoffdioxidemissionen und die Bereitstellung von Elektroenergie nach Bedarf, kommen allerdings nur dann zum Tragen, wenn die Bereitstellung von Wasserstoff als Brennstoff zufriedenstellend gelöst ist.
Die einfachste Variante für die Gewinnung von Wasserstoff wäre die Elektrolyse von Wasser. Wird der dafür benötigte Strom aber wie bisher in Kohlekraftwerken erzeugt, sind die Emissionen nur verlagert. Daher müsste die Elektroenergie für die Wasserstofferzeugung im Sinne eines nachhaltigen Energiekonzepts auf der Basis regenerativer Energiequellen (z. B. Windenergie, Fotovoltaik) erzeugt werden. Ein Problem dabei ist, dass es je nach Windstärke oder Sonnenscheindauer erhebliche Schwankungen in der Stromerzeugung geben kann und Spitzenzeiten in der Stromerzeugung nicht mit solchen im Bedarf übereinstimmen. Zum Ausgleich dienen Speicher, z. B. Akkumulatoren oder chemische Speicher wie Wasserstoff. Weiterhin sind Stromerzeuger und Stromverbraucher räumlich getrennt.
Der elektrolytisch erzeugte Wasserstoff kann nun dabei eine Doppelfunktion übernehmen. Einerseits fungiert er als Energiespeichermedium, zum anderen kann man mittels Wasserstoff gespeicherte Elektroenergie zum Verbraucher (z. B. Automobil) transportieren und dort zu beliebigen Zeiten dann über Brennstoffzellen zurückgewinnen.
Für dieses Konzept einer globalen Wasserstoffwirtschaft in einem regenerativen Energieverbundsystem sind aber noch viele Probleme zu lösen. Eines davon ist die sichere Lagerung sowie der Transport großer Mengen an Wasserstoff.
-
Auto mit Brennstoffzellenantrieb

-
Prinzip einer modernen Brennstoffzelle (Tieftemperatur-Brennstoffzelle)
-
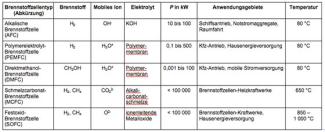
Verschiedene Brennstoffzellentypen im Überblick
Suche nach passenden Schlagwörtern
- Reformierung
- Anode
- galvanisches Element
- Katode
- Mitteltemperaturbrennstoffzelle
- Niedertemperaturbrennstoffzellen
- Elektroautos
- Nachteile
- Raumfahrt
- Polymer-Elektrolytmembran-Brennstoffzelle
- William Grove
- Vorteile
- Gesamtelektrodenreaktion
- Membran
- Hochtemperaturbrennstoffzelle
- Halbzellen
- Kraftwerke
- Fahrzeugantrieb
- Elektroden
- Brennstoffzelle

