Projekt Bierherstellung
Die Technik des Bierbrauens von der Gerste bis zum Bier als umfasst weit mehr als den Prozess der alkoholischen Gärung. Der biochemische Hintergrund kann im Chemieunterricht durch eine Reihe von Experimenten untersucht werden. Im Rahmen des Projektes wird die Geschichte der Bierbrauerei und die moderne Technologie der Bierherstellung erläutert.
Bier - ein Getränk mit Geschichte
Das liebste Getränk der Deutschen ist schon seit Tausenden Jahren bekannt. Schon bei den Ägyptern galt Bier als Volksgetränk und wurde auch den Sklaven als Nahrungsmittel ausgeschenkt. Bei den alten Germanen wurde vor jeder Versammlung Bier getrunken, da man annahm, dass die alkoholisierende Wirkung des Bieres der Redseeligkeit und der Wahrheitsfindung diente.
Der Brauvorgang selbst dürfte eher zufällig entdeckt worden sein. Denkbar wäre, dass feuchtes Brot in einem Tongefäß vergessen und später der entstandene Brei verkostet wurde. Zum Erstaunen stellte man eine berauschende Wirkung dieses süß-säuerlich schmeckenden Breies fest. Wahrscheinlich haben Wildhefen den Gärvorgang initiiert. Dieser Prozess könnte dann verändert und verbessert worden sein. Die Brot-Biere waren trübe, enthielten noch keinen Hopfen und waren nur begrenzt haltbar.
Die Bierherstellung wurde vor allem in Klöstern weiterentwickelt und dafür die verschiedensten Rohstoffe verwendet. Aufgrund der wahllos zusammengestellten Zutaten, deren sich die Brauer bedienten, erließ 1516 der Herzog Wilhelm IV. von Bayern das Deutsche Reinheitsgebot . In dieser ältesten Lebensmittelverordnung der Welt schützt der Herzog nicht nur die bayerischen Biertrinker vor allerlei obskuren Zutaten, sondern regelt auch den Preis, zu dem die Brauer das Bier maximal verkaufen dürfen: „… Wo aber einer nicht Märzen - sondern anderes Bier brauen oder sonstwie haben würde, soll er es keineswegs höher als um einen Pfennig die Maß ausschenken und verkaufen. Ganz besonders wollen wir, dass forthin allenthalben in unseren Städten, Märkten und auf dem Lande zu keinem Bier mehr Stücke als allein Gersten, Hopfen und Wasser verwendet und gebraucht werden sollen. Wer diese unsere Androhung wissentlich übertritt und nicht einhält, dem soll von seiner Gerichtsobrigkeit zur Strafe dieses Fass Bier, so oft es vorkommt, unnachsichtlich weggenommen werden.“
Erst 1876 klärte der französische Wissenschaftler LOUIS PASTEUR in seinem Werk „Etudes sur la biere“ die biochemischen Vorgänge der Bierherstellung auf. Er konnte nachweisen, dass für den alkoholischen Gärprozess Hefen verantwortlich sind. Später erkannte EDUARD BUCHNER (1860¯-1917), dass die von den Hefen produzierten Enzyme eine Schlüsselrolle bei der alkoholischen Gärung spielen.
Nach dem bis heute gültigen Reinheitsgebot dürfen zur Bierherstellung nur Gerste, Wasser, Hopfen und die später dazugekommene Hefe als Rohstoffe zur Bierherstellung verwendet werden. Heute existieren in Deutschland über 5 000 verschiedene Biersorten, die sich alle nur in Menge, Verarbeitung und Qualität ihrer Zutaten unterscheiden dürfen. Die Technik des Bierbrauens von der Gerste bis zum Bier als „Gerstensaft“ umfasst weit mehr als den Prozess der alkoholischen Gärung (Bild 9, siehe unten), kann aber trotzdem im Chemieunterricht anschaulich nachgestellt werden.
Von der Gerste zu Maische
Ein Gerstenkorn besteht aus der Frucht- und Samenschale, der Aleuronschicht, dem Nährgewebe und dem Keimling. Frucht- und Samenschale dienen dem Korn als Schutz. Die Aleuronschicht enthält Eiweiße, Fette, Mineralsalze und Vitamine. Das Nährgewebe liefert dem Keimling die nötige Energie zum Wachstum.
Das Nährgewebe (ca. 85 %) ist mit Stärkekörnchen angefüllt. Zwischen der Stärke befinden sich Eiweiße sowie geringe Mengen löslicher Zucker, Fette und 0,3 bis 0,5 % Mineralsalze. Stärke gehört zu den Kohlenhydraten (Zuckern) und kann mit Iod-Kaliumiodid-Lösung nachgewiesen werden.
-
Gerste liefert das Kohlenhydrat Stärke als Ausgangsstoff für den Brauprozess.
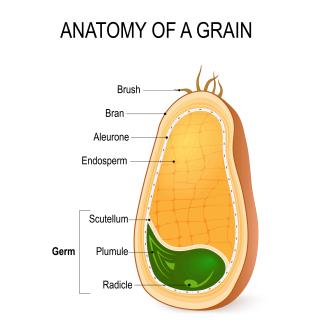
Designua - shutterstock
Experiment 1
Aufgabe:
Weise Stärke im Gerstenkorn nach.
Vorbereitung:
Geräte: Mörser mit Pistill, Objektträger, Deckgläschen, Filterpapier, Pipette
Chemikalien: Iod-Kaliumiodid-Lösung, Wasser, Gerstenkörner
Durchführung:
Zermörsere einige Gerstenkörner, bis du ein feines Schrot erhältst und füge etwas Wasser hinzu. Gib mit der Pipette einen Tropfen des Gemisches auf einen Objektträger und lege ein Deckgläschen darauf. Um die Strukturen der Stärke besser erkennbar zu machen, färbe das Präparat mit Iod-Kaliumiodid-Lösung an. Dazu pipettierst du einen Tropfen der Färbelösung an den Rand des Deckgläschens und saugst den Tropfen mithilfe von Filterpapier durch das Präparat.
Beobachtung und Auswertung:
Notiere deine Beobachtungen und fertige ein farbiges mikroskopisches Bild der Stärkekörner an.
Fügt man einer Stärkelösung Hefe zu, so wird man feststellen, dass die Hefe keine Gärtätigkeit entwickelt. Stärke kann also nicht direkt zu Ethanol und Kohlenstoffdioxid vergoren werden. Die Ursache liegt im Bau der Stärkemoleküle. Stärke ist ein Vielfachzucker, dessen Moleküle aus vielen Baueinheiten von Glucose bestehen. Der Vielfachzucker muss erst in kleinere Baueinheiten aus zwei Glucosebausteinen zerlegt werden, damit er mit der Hefe reagieren kann. Im Getreide sind Enzyme vorhanden, die Stärke zu einem vergärbaren Zweifachzucker, der Maltose (Malzzucker) abbauen können. Diese chemische Reaktion lässt sich durch folgendes Experiment nachweisen.
-
Bau verschiedener Kohlenhydrate (Zucker)
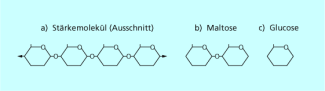
Experiment 2
Aufgabe:
Vergleiche Malz und Gerste auf ihren Malzzuckergehalt.
Vorbereitung:
Geräte: 2 Mörser mit Pistill, Löffel, 3 Reagenzgläser, Reagenzglasständer, Reagenzglasklammer, Bunsenbrenner, Vierfuß mit Ceranplatte, Becherglas, Schutzbrille
Chemikalien: Malzzucker (Maltose), Gerste, Malz, fehlingsche Lösung I und II, Wasser
Durchführung:
Gib in einen Mörser einen Löffel voll Gerste, in den anderen einen Löffel Malz. Zerkleinere beides mit Hilfe der Pistille.
Gib anschließend eine Spatelspitze des Malzzuckers in Reagenzglas 1, eine Spatelspitze des Gerstenmehls in Reagenzglas 2 und eine Spatelspitze des Malzmehls in Reagenzglas 3.
Nun fülle in jedes Reagenzglas jeweils ca. 2 cm hoch fehlingsche Lösung I und II ein und erhitze anschließend vorsichtig im Wasserbad (Schutzbrille aufsetzen!).
Beobachtung und Auswertung:
Notiere deine Beobachtungen und erkläre sie. Erstelle ein Fließschema, das den Abbau der Stärke bis zum Ethanol bei der Bierherstellung wiedergibt.
Mit der Hefe zur Gärung
Der Abbau von Stärke zu Maltose geschieht in der Mälzerei und ist der erste Schritt der Bierherstellung. Das Malz wird getrocknet und an die Brauerei geliefert. Hier wird es zu Schrot gemahlen und mit Wasser zur Maische vermischt (Bild 9, siehe unten).
Der wasserlösliche Malzzucker aus der Maische muss nun vergoren werden. Dazu filtriert man die Maische und fügt Hopfen zum Filtrat, dass der Brauer Würze nennt. Als fester Rückstand bleibt sogenannter Treber zurück, der als Kraftfutter für Schweine genutzt wird. Die Würze versetzt man anschließend mit Hefe , um die Kohlehydrate zu vergären. Die Bierhefen (Saccharomyces cerevisiae und Saccharomyces carlsbergensis) gehören zu den Sprosspilzen. Dabei handelt es sich um einzellige, kugelige Pilze von 5 bis 15 pm Größe. Im Lichtmikroskop lassen sie kaum Details erkennen. Erst durch Anfärben mit spezifischen Farbstoffen werden die Zellbestandteile sichtbar.
-
Nachweis von Maltose und Glucose mit fehlingscher Lösung (Vorsicht! Siedeverzug!)
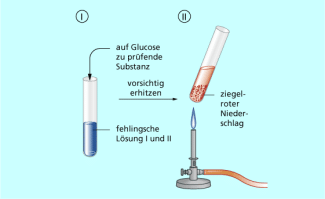
Experiment 3
Aufgabe:
Fertige ein mikroskopisches Bild der Hefe an.
Vorbereitung:
Geräte: Mikroskop, Objektträger, Deckgläschen, Pipette, Becherglas (50 ml), Spatel
Chemikalien: Trockenhefe, lauwarmes Wasser, Traubenzucker
Durchführung:
Gib eine Spatelspitze Trockenhefe und dieselbe Menge Traubenzucker in das Becherglas. Fülle es zur Hälfte mit Wasser auf und rühre gut um.
Gib einen Tropfen der Suspension auf einen Objektträger, setze ein Deckgläschen rauf und betrachte das Präparat unter dem Mikroskop. Beginne mit der kleinsten Vergrößerung.
Beobachtung und Auswertung:
Notiere deine Beobachtungen. Versuche, eine Zellteilung zu erkennen und beschreibe den Vorgang.
Die Hefezellen enthalten bzw. produzieren selbst verschiedene Enzyme , die den biochemischen Abbau von Maltose zu Glucose und die Vergärung der Zucker ermöglichen bzw. beschleunigen. Auf diese Weise können Hefezellen die Energie für Wachstum und Vermehrung gewinnen, wenn kein Sauerstoff zur Verfügung steht.
In Gegenwart von Sauerstoff (unter aeroben Bedingungen, z. B. an der Luft) bauen Hefen Kohlenhydrate durch Atmung vollständig zu Kohlenstoffdioxid und Wasser ab:
-
Hefezellen vermehren sich asexuell durch Zellteilung (Sprossung).

Yuliya_Lesovaya - iStock
Bei der Atmung werden die Hefeenzyme nicht benötigt. Steht jedoch kein Sauerstoff zur Verfügung (anaerobe Bedingungen), dann stellen die Hefezellen ihren Stoffwechsel um. Unter Beteiligung der Enzyme erfolgt nur ein unvollständiger Abbau von Traubenzucker durch alkoholische Gärung zu Ethanol und Kohlenstoffdioxid.
Die Gärung ist wie die Atmung ein exothermer Prozess. Zwar wird bei der Gärung ein deutlich geringerer Energiegewinn erzielt (2 ATP statt 18 ATP), aber der Zelle dadurch das Überleben unter Sauerstoffausschluss ermöglicht.
Der Alkohol (Ethanol) kann von den Hefezellen nicht weiter verarbeitet werden und wird ausgeschieden. Dabei vertragen sie nur einen Alkoholgehalt von ungefähr 15 %, da Ethanol auch für Hefezellen giftig ist und diese bei höheren Konzentrationen absterben.
Der Verlauf des Gärprozess ist von mehreren Reaktionsbedingungen abhängig. Das folgende Experiment zeigt die Temperaturabhängigkeit der alkoholischen Gärung
Experiment 4
Aufgabe:
Triff eine Voraussage zur Temperaturabhängigkeit der Gärung und überprüfe deine Vermutung experimentell.
Vorbereitung:
Geräte: 3 Gärröhrchen nach EINHORN, 3 Bechergläser (50 ml), Spatel
Chemikalien: Trockenhefe, Wasser, Traubenzucker
Durchführung:
Gib zwei Spatelspitzen Trockenhefe und zwei Spatelspitzen Traubenzucker in jedes der drei Bechergläser. Fülle jeweils zur Hälfte mit Wasser auf und rühre gut um. Befülle jeweils ein Gärröhrchen mit der Suspension. Stelle einen Ansatz in den Kühlschrank (ca. 10 °C), einen in den Trockenschrank (40°C) und einen auf die Fensterbank (ca. 20 °C).
Beobachtung und Auswertung:
Notiere deine Beobachtungen in der nächsten Chemiestunde und erkläre sie. Wurde deine Voraussage bestätigt?
-
Unter anaeroben Bedingungen gewinnen Hefezellen durch alkoholische Gärung Energie.
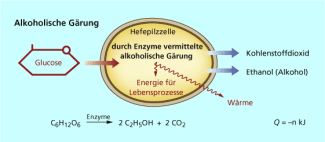
Technologie der Bierherstellung
Der allgemeine technologische Ablauf der Bierherstellung ist in Bild 9 dargestellt: Das in der Mälzerei produzierte Malz wird zuerst in einer Schrotmühle zerkleinert (Schroten). Bei der Einmaischung wird das geschrotete Malz mit dem Brauwasser bei einer Temperatur von 35°C bis 50°C unter ständigem Rühren in der Maischpfanne vermischt.
Bei dieser Temperatur erfolgt der Eiweißabbau. Die Dauer und Temperatur ist entscheidend für die Klärung, die Schaumbildung und die Vollmundigkeit des Bieres. Dann erhöht man die Temperatur auf 60 bis 74 °C , um die verbleibende Stärke zu Malzzucker (Maltose) abzubauen. Durch eine Temperaturerhöhung auf 78°C wird die Stärke vollständig in Maltose umgewandelt.
Als Läutern bezeichnet der Brauer die Trennung (Filtrierung) des festen Malzschrotes (Treber) von der verbleibenden Flüssigkeit (Würze). Die noch heiße Würze wird je nach Bierart mit unterschiedlichen Mengen Hopfen vermischt und gekocht. Anschließend filtriert man die gehopfte Würze, um diese von den entstandenen Trübstoffen zu trennen.
Zur Gärung wird die gehopfte Würze auf die je nach Biersorte notwendige Gärtemperatur abgekühlt und mit entsprechender Bierhefe versetzt. Die Gärung dauert ca. eine Woche. Zur Nachreifung lagert die Brauerei das fertige aber noch junge Bier 4 bis 5 Wochen in großen Tanks. Danach wird es noch einmal gefiltert, in Fässer bzw. Flaschen abgefüllt und verkauft.
-
Die Herstellung von Bier erfolgt in allen Brauereien prinzipiell ähnlich.
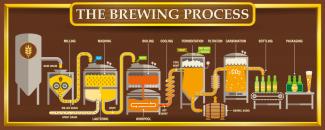
alejomiranda - iStock
Bei der Ausarbeitung und Erprobung des Projekts zum Thema „Bierherstellung im Chemieunterricht“ bedanken wir uns bei den Schülerinnen und Schülern der Klassen 11a und 11d und ihrem Chemielehrer Herrn Bernd Sauer des Gymnasiums Berlin-Steglitz sowie bei den Klassen E1 und E3 un ihrem Chemielehrer Herrn Jens Bussen der Friedrich-Ebert-Oberschule aus Berlin im Schuljahr 2004/2005.

