Sauerstoff Verbindungen
Sauerstoff ist ein Element der VI. Hauptgruppe und bildet mit fast allen Elementen des Periodensystems stabile Oxide. Als Bestandteil der Oxide und anderer Verbindungen (z. B. Silicate, Carbonate) ist Sauerstoff das häufigste Element der Erdkruste. Reaktionen unter Beteiligung von Sauerstoff wie die Verbrennung von Kohle oder von Kohlenhydraten (Atmung) sind wichtige Prozesse in Natur und Technik. Solche Prozesse bezeichnet man als Oxidationsreaktionen.
Der Luftsauerstoff und das häufigste Elementoxid, das Wasser, ermöglichen erst das Leben auf der Erde. Aber auch viele technisch wichtige Werkstoffe wie Glas (Siliciumdioxid), Keramiken (Aluminiumoxid) oder Erze (Eisenoxid) sind Oxide. Aus der Reaktion der Oxide mit Wasser entstehen entweder Säuren oder Basen.
Sauerstoff ist ein Element der VI. Hauptgruppe. Das Element Sauerstoff wurde 1771 von C. W. SCHEELE entdeckt. Das Sauerstoffatom besitzt 8 Protonen und meist 8 Neutronen im Atomkern sowie 8 Elektronen in der Atomhülle. Auf der ersten Elektronenschale befinden sich zwei und auf der zweiten Elektronenschale sechs Elektronen, sodass Sauerstoff über sechs Außenelektronenelektronen verfügt.
Um eine stabile Elektronenanordnung, die Achterschale des Neons zu erreichen, muss ein Sauerstoffatom zwei Elektronen von Bindungspartnern aufnehmen. Mit elektropositiven Bindungspartnern wie Metallen bildet Sauerstoff ionische Verbindungen, die Sauerstoff-Anionen, , enthalten. Mit den elektronegativeren Nichtmetallen wie Kohlenstoff oder Schwefel wird das Elektronenoktett durch die Ausbildung polarer Atombindungen erreicht.
Sauerstoffatome können untereinander ebenfalls Atombindungen eingehen und auf diese Weise Moleküle bilden. Die gewöhnliche Erscheinungsform ist der zweiatomige Disauerstoff, der zu ca. 21 Vol-% in der Luft enthalten ist.
Die beiden Atome im Disauerstoffmolekül sind durch zwei gemeinsame Elektronenpaare (unpolare Atombindung) miteinander verbunden. Jedes Sauerstoffatom besitzt noch vier nicht bindende Elektronen, d. h. je zwei freie Elektronenpaare.
Überraschenderweise ist molekularer Sauerstoff paramagnetisch. Nach der einfachen Vorstellung, dass die beiden Sauerstoffatome durch zwei Elektronenpaare in einer Doppelbindung im Molekül miteinander verbunden sind, sollte man Diamagnetismus erwarten. Der Paramagnetismus des Sauerstoffmoleküls kann aber mittels der MO-Bindungstheorie erklärt werden.
Das Element Sauerstoff ist ein farbloses, geruchloses, Gas. Sauerstoff ist selbst nicht brennbar, fördert jedoch die Verbrennung. Es ist lebenswichtiger Bestandteil der Luft, da es für den biochemischen Prozess der Atmung benötigt wird.
Eine zweite Modifikation des Sauerstoffs ist das Ozon, das aus gewinkelten -Molekülen besteht. Ozon ist ebenfalls ein Gas, sein Schmelz- und Siedepunkt liegen aber höher als der von und es ist deutlich reaktiver als der gewöhnliche Sauerstoff.
Ozon ist ein bläuliches, giftiges Gas, dessen charakteristischen Geruch, man z. B. gut in Copyshops wahrnehmen kann. Es zerfällt bei Energiezufuhr (Licht, Wärme) sehr schnell zu Sauerstoff.
Die Bildung von Ozon aus Sauerstoff ist endotherm. Es entsteht z. B. in den höheren Luftschichten der Atmosphäre aus Sauerstoffmolekülen, die durch UV-Strahlung angeregt wurden, und bildet die schützende Ozonschicht. Diese ist für uns wichtig, weil sie UV-Strahlung, die uns schaden würde, von der Erdoberfläche fernhält.
In Bodennähe führen Autoabgase im Sommer zur Bildung von Ozon, das wesentlichen Anteil am Sommersmog hat. Hier ist es nicht erwünscht, weil es Augen und Schleimhäute reizt und die Atmungsorgane schädigt.
-
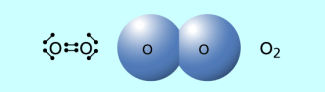
Valenzstrichformel und Kalottenmodell des Sauerstoffmoleküls
Reaktionen des Sauerstoffs
Sauerstoff ist ein typisches Nichtmetall. Da die Atombindungen im Sauerstoffmolekül relativ stark sind, reagiert das Gas bei Zimmertemperatur nur mit wenigen Reaktionspartnern, z. B. unedlen Metallen oder Phosphor. Bei höheren Temperaturen werden jedoch mit nahezu allen Elementen die Oxide unterschiedlicher Zusammensetzung als Element-Sauerstoff-Verbindungen gebildet. Die in der Regel exotherme Reaktion bezeichnet man als Verbrennung , sie verläuft wie die Knallgasreaktion zwischen Wasserstoff und Sauerstoff in vielen Fällen sehr heftig.
Nicht nur andere Elemente, sondern auch viele Verbindungen reagieren unter Freisetzung von Wärme mit Sauerstoff. Allgemein nennt man die Reaktion eines Stoffes mit Sauerstoff auch Oxidation. Eingeführt wurde dieser Begriff von A. DE LAVOISIER im Jahre 1774. In der modernen Chemie ist der Begriff Oxidation allerdings nicht mehr allein auf die Anlagerung von Sauerstoff beschränkt.
Sauerstoff kommt molekular mit ca. 21 Vol-% in der Luft vor. In anorganischen Verbindungen tritt Sauerstoff in Form von Silicaten, Carbonaten in Gesteinen oder Oxiden, z. B. Sand () und Wasser (), auf. Mit einem Anteil von fast 50 % ist Sauerstoff das bei weitem häufigste Element in der Erdkruste.
Auch viele organischen Verbindungen wie Kohlenhydrate, Alkohole oder Carbonsäuren enthalten Sauerstoff im Molekül.
Sauerstoff kann neben Wasserstoff durch elektrolytische Zersetzung des Wassers gewonnen werden. Eine weitere Möglichkeit, reinen Sauerstoff herzustellen, besteht darin, Luft zu verflüssigen und durch Destillation bei tiefen Temperaturen die Bestandteile Stickstoff und Sauerstoff zu trennen.
-
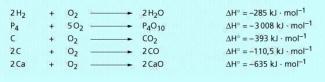
Reaktionen verschiedener Elemente mit Sauerstoff
Reiner Sauerstoff wird z. B. in der Medizin in Beatmungsgeräten eingesetzt. Im Gemisch mit brennbaren Gasen wird das Gas zum Schweißen und Brennschneiden genutzt. Sauerstoff wird zur Stahlerzeugung aus Roheisen verwendet. Durch Einblasen von Sauerstoff in das flüssige Roheisen werden der Kohlenstoff und andere störende Verunreinigungen oxidiert und ausgetrieben. Man benötigt ihn auch für Oxidationsreaktionen in der organischen Chemie. Flüssiger Sauerstoff wird als Raketentreibstoff genutzt. Weiterhin findet er Anwendung beim Bleichen und in der biologischen Abwasserreinigung.
Anorganische Sauerstoffverbindungen
Oxide sind chemische Verbindungen, in denen das Element Sauerstoff mit mindestens einem weiteren Element verbunden ist. Sie entstehen durch die Verbrennung von Elementen mit Sauerstoff, aber auch durch Redoxreaktionen oder Entwässerung von Hydroxiden oder geeigneten Salzen:
Viele Elemente können wie Stickstoff Oxide verschiedener Zusammensetzung bilden. Nach der Anzahl der im Molekül vorhandenen Sauerstoffatome werden Monooxide, Dioxide, Trioxide, Tetraoxide usw. benannt.
Wichtige Oxide sind einige Metalloxide, wie Aluminiumoxid oder Eisenoxid aus denen die Metalle gewonnen werden. Einige Metalloxide wie Chrom(III)-oxid oder Kupfer(II)-oxid werden als farbgebende Oxide in der Glasindustrie genutzt. Nichtmetalloxide, wie Schwefeldioxid, , oder die Stickstoffoxide und werden zur Herstellung der Säuren benötigt. Als Bestandteile von Abgasen schädigen diese Oxide die Umwelt durch den sauren Regen.
Das am häufigsten vorkommende Oxid ist Wasser . Im Wassermolekül sind zwei Wasserstoffatome mit einen Sauerstoffatom miteinander verbunden. Wasser ist ein amphoteres Oxid. Es kann als Brönsted-Säure oder als Brönsted-Base reagieren. Durch seinen Dipolcharakter ist Wasser eines der besten Lösungsmittel für alle polaren Verbindungen und Ionensubstanzen.
-
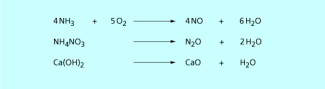
Bildung von Oxiden durch Redoxreaktionen oder Entwässerung
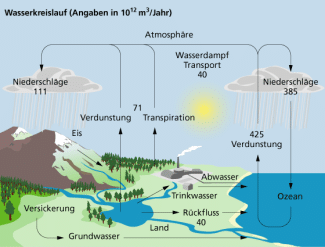
Wasser kommt auf der Erde nicht nur in flüssiger Form, sondern auch als Eis oder als Wasserdampf in der Atmosphäre vor. Die Zirkulation des Wassers wird im Wasserkreislauf beschrieben. Wasser ist ein universelles Lösungsmittel, Lebensraum, Baustoff aller Lebewesen, Transportmittel und Nährstoff. Die Wasservorkommen der Erde werden auf insgesamt 1,4 Mrd. Kubikkilometer geschätzt.
-
Kreislauf des Wassers
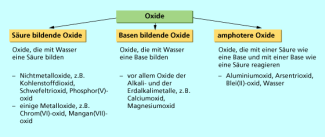
Ein wichtiges Merkmal zur Einteilung der Oxide ist ihr Reaktionsverhalten gegenüber Wasser. Danach unterscheidet man zwischen sauren, basischen und amphoteren Oxiden (Bild 7).
Durch die Reaktion mit Wasser entstehen weitere anorganische Verbindungen des Sauerstoffs, die sauerstoffhaltigen Säuren, ihre Salze oder Hydroxide (Basen).
Peroxide
In fast allen Verbindungen mit anderen Elementen, die Ausnahme sind die Sauerstofffluoride, besitzt Sauerstoff die Oxidationsstufe (-2). Sauerstoff bildet aber auch Verbindungen mit der Oxidationsstufe (-1), die Peroxide mit einer O-O-Gruppe. Die bekannteste Verbindung ist das Wasserstoffperoxid H2O2 mit der Struktur H-O-O-H, beide Sauerstoffatome haben die Oxidationsstufe (-1). Es gibt auch ionische Peroxide wie das Natriumperoxid Na2O2 mit Peroxo-Ionen O2 2- im Gitter.
Die Eigenschaften der anorganischen Säuren und Basen sind in den entsprechenden Beiträgen umfassend beschrieben.
-
Einteilung der Oxide nach ihrem Reaktionsverhalten