Stickstoffkreislauf
Stickstoff ist eines der Elemente, das alle Lebewesen der Erde für körpereigene Eiweiße benötigen.
Der mit den Lebewesen verknüpfte Kreislauf des Stickstoffs lässt sich in vier Abschnitte unterteilen: Fixierung des Luftstickstoffs, Assimilation von Stickstoff in Pflanzen, Umwandlung von organischen Stickstoffverbindungen und Umwandlung von organischen Stickstoffverbindungen in anorganische.
Stickstoff und stickstoffhaltige Verbindungen sind in einen Kreislauf eingebunden (Bild 2). Stickstoff ist eines der Elemente, welches alle Lebewesen der Erde für den Aufbau körpereigener Eiweiße benötigen.
Eigentlich ist das Element Stickstoff in der Atmosphäre in ausreichendem Maße vorhanden.
Der molekulare Stickstoff ist allerdings so reaktionsträge, dass er nicht von Organismen direkt aufgenommen werden kann. Die Schmetterlingsblütengewächse (Leguminosen) z. B. leben in Symbiose mit Knöllchenbakterien, die in der Wurzel dieser Pflanzen knöllchenartige Verdickungen hervorrufen. Diese Bakterien sind in der Lage den Luftstickstoff direkt in der Wurzel in stickstoffhaltige Salze, z. B. Ammonium- und Nitrat- Ionen umzuwandeln, sodass die Pflanze diese Ionen nicht mehr aus dem Boden aufnehmen muss. Die Schmetterlingsblütengewächse können aufgrund dieser Symbiose auf stickstoffarmen Böden wachsen. Das bedeutendste Beispiel für die sogenannte biologische Fixierung sind blaugrüne Algen im Wasser. Sie wandeln den molekularen Stickstoff in Ammoniak um.
Bei Gewittern kommt es durch die Energie der elektrischen Entladungen zur Bildung von Stickstoffoxiden in der Luft.
Da in der Luft stets Wasserdampf enthalten ist lösen sich diese Oxide im Wasser zu den entsprechenden Säuren. Der Regen enthält deshalb immer einen Anteil an Salpetersäure und Salpetriger Säure, die dann weiter zu Salpetersäure oxidiert wird. Gelangen Niederschläge mit Spuren von Salpetersäure in den Erdboden, bilden sich die Salze der Salpetersäure, die Nitrate. Dieser Ablauf wird auch als atmosphärische Fixierung bezeichnet.
Nitrate und Nitrite entstehen jedoch im Boden vor allem durch die Bodenbakterien, welche diese in ihrem Stoffwechsel herstellen, z. B. durch dem Abbau toter organischer (eiweißhaltiger) Substanz.
Die Eiweiße werden dabei zunächst in Ammoniumverbindungen und danach in Nitrite und Nitrate umgewandelt.
Nitrate werden in gelöster Form von den Pflanzen besonders gut aufgenommen und u. a. zum Aufbau von Eiweißen verwertet. Diesen Vorgang bezeichnet man auch als Assimilation.
Ein geringerer Teil der Nitrate wird weiter zu molekularem Stickstoff abgebaut (Denitrifikation), der in die Atmosphäre gelangt.
-
Knöllchenbakterien in Wurzeln von Schmetterlingsblütengewächsen können Luftstickstoff binden.

-
Stickstoffkreislauf in der Natur
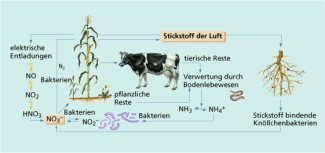
Der mit den Lebewesen verknüpfte Ablauf des Stickstoffkreislaufs lässt sich in vier Abschnitte unterteilen
- Fixierung des Luftstickstoffs:
Nur bestimmte Bakterien besitzen die passenden Enzyme, um den molekularen Stickstoff der Luft zu Ammoniak (Ammonium-Ionen) umzuwandeln. In einem zweiten Schritt wird Ammoniak dann von anderen Bakterienarten zu Nitrit- und Nitrat-Ionen oxidiert.
Die Oxidation zu Nitrit- und weiter zu Nitrat-Ionen wird als Nitrifikation bezeichnet.
Die ablaufenden chemischen Reaktionen können mit folgendem Schema wiedergegeben werden.
- Assimilation von Stickstoff in Pflanzen:
Die meisten höheren Pflanzen nehmen mit dem Wasser aus dem Boden auch darin gelöste Ionen, z. B. Ammonium-, Nitrit- und Nitrat-Ionen auf. Der Stickstoff in diesen Ionen wird u. a. zum Aufbau der Aminosäuren benötigt.
Aus diesen bildet sich pflanzliches Eiweiß.
- Umwandlung von organischen Stickstoffverbindungen:
Tiere nehmen Eiweiße von Pflanzen oder anderen Tieren mit der Nahrung auf, zerlegen diese im Stoffwechsel und wandeln sie in körpereigene organische Stickstoffverbindungen um.
- Umwandlung von organischen Stickstoffverbindungen in anorganische – Zersetzung::
Von Tieren ausgeschiedene organische Stickstoffverbindungen sowie die gesamte tote organische Substanz werden durch Bakterien und Pilze zersetzt. Die Mikroorganismen wandeln Eiweiße und andere stickstoffhaltige Verbindungen mithilfe von Sauerstoff in Ammoniumverbindungen (Ammonifikation) und andere anorganische Verbindungen um. Dieser Vorgang wird Verwesung genannt. Aus den Ammonium-Ionen werden durch Nitrifikation wieder Nitrit- und Nitrat-Ionen. Auch gasförmiges Ammoniak kann aus dem Boden entweichen.
Bei der Nitrifikation wird aber ein Teil des Ammonium-Stickstoffs in Distickstoffmonooxid N2O (Lachgas) umgewandelt, das in die Atmosphäre entweicht. Dieses Gas ist wie Kohlenstoffdioxid ein Treibhausgas.
Durch die industrielle Stickstoff-Fixierung, die Synthese von Ammoniak über den Haber-Bosch-Prozeß und dessen Weiterverarbeitung zu Stickstoffdüngemitteln für die Landwirtschaft, übt der Mensch einen bedeutenden Einfluß auf den natürlichen Stickstoffkreislauf aus.
Zwar wird der größte Teil des verabreichten Stickstoffdüngers von den Pflanzen aufgenommen, aber damit sind auch die Emissionen des Treibhausgases Distickstoffmonooxid in den letzten Jahrzehnten erheblich angestiegen.
Das andere Problem ist, dass Nitrat als Anion im Gegensatz zu Ammonium-Ionen nicht an Bodenbestandteilen wie den Huminsäuren gebunden wird. Dadurch kann es leicht in tiefere Bodenschichten oder in das Grundwasser ausgewaschen werden. In den letzten Jahrzehnten ist die Zahl der Brunnen zur Trinkwassergewinnung in Deutschland gewachsen, die kritische Nitratgehalte aufweisen. Höhere Nitratgehalte sind aber gesundheitlich bedenklich, weil Nitrat im Körper mit körpereigenen Aminen zu Stoffen reagieren kann, die Krebs auslösen.
Für Babys sind erhöhte Nitratgehalte im Trinkwasser besonders gefährlich, weil dadurch das Eisen im Hämoglobin in eine Form überführt wird, die den Sauerstoff nicht mehr aufnehmen kann. Die Folge ist, dass die Babys ersticken.
-
Stickstoffkreislauf (schematisch)
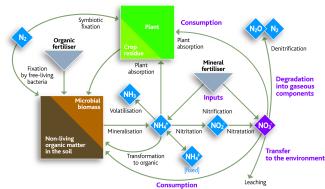
Graphithèque - adobe stock

