Amine
Amine sind organische Stickstoffverbindungen mit der Amino-Gruppe als funktioneller Gruppe. Sie weisen ähnliche chemische Eigenschaften wie Ammoniak auf und können vereinfacht als Abkömmlinge (Derivate) des Ammoniaks betrachtet werden.
Amine haben sowohl in der chemischen Industrie als auch in der Natur große Bedeutung. Einige sind lebensnotwendig, andere sehr giftig. In der Industrie werden Amine als Ausgangsstoffe oder Zwischenprodukte wichtiger technischer Verfahren genutzt.
Von ihrer Struktur her kann man Amine als Derivate des Ammoniaks auffassen, unabhängig davon, wie viele Wasserstoffatome des Ammoniaks durch organische Reste (R) ersetzt sind.
Betrachtet man die Amine dagegen als Abkömmlinge (Derivate) von Kohlenwasserstoffen, dann sind ein oder mehrere Wasserstoffatome des Kohlenwasserstoffs durch die Amino-Gruppe ersetzt.
Aufgrund des freien Elektronenpaars am Stickstoffatom der funktionellen Amino-Gruppe sind die chemischen Eigenschaften der Amine denen des Ammoniak sehr ähnlich.
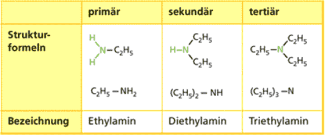
Die Verbindungen tragen im Namen den Wortteil -amin. Man unterscheidet je nach Art der organischen Reste am Stickstoff zwischen aliphatischen oder aromatischen Aminen. Je nach Anzahl der Reste am Stickstoffatom unterteilt man in primäre, sekundäre bzw. tertiäre Amine (Bild 2).
Die kettenförmigen, aliphatischen Amine sind bei Zimmertemperatur gasförmige oder flüssige Verbindungen. Sie haben einen fischartigen, dem Ammoniak ähnlichen Geruch. Sie sind gut wasserlöslich, wobei mit steigender Kettenlänge die Wasserlöslichkeit abnimmt.
Aromatische Amine besitzen eine hohe Toxizität und werden durch die Haut schnell aufgenommen. Der Grundkörper der aromatischen Amine ist das Aminobenzen (Anilin).
Reaktion mit Wasser
An das freie Elektronenpaar der Amino-Gruppe lagern sich sehr leicht Protonen an, d. h. die Amine reagieren in wässrigen Lösungen basisch.
![]()
Auch gegenüber anderen Reaktionspartnern verhalten sich Amine wie Basen. Mit Säuren bilden Amine Ammoniumsalze.
-
Einteilung der Amine
Wichtige Amine
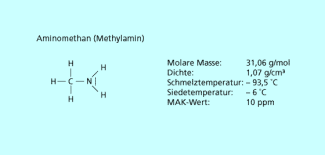
Das Aminomethan (Methylamin) ist der einfachste Vertreter der Amine (Bild 3). Es handelt sich um ein brennbares, farbloses Gas, das in verdünnter Form nach Fisch riecht.
Es bildet mit Luft explosive Gemische. Die Zündtemperatur beträgt 430 °C. Das Gas ist in Wasser und Ethanol gut löslich, reagiert basisch und reizt Atemwege, Haut und Augen bei längerem Kontakt oder in höheren Konzentrationen.
Methylamin wird in der chemischen Industrie oder im Labor oft als Überträger von Aminogruppen benutzt. Auch als Neutralisationsmittel und in der Gerberei wird es eingesetzt.
-
Struktur und Eigenschaften von Aminomethan
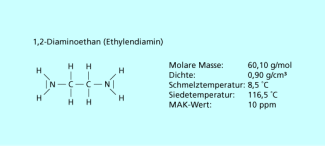
Das 1,2-Diaminoethan (Ethylendiamin) ist eine farblose, nach Ammoniak riechende, stark alkalische Flüssigkeit. Sie ist löslich in Wasser und Ethanol. Ihre Dämpfe reizen die Atemwege und Augen. Bei Kontakt mit dem flüssigen Diaminoethan kommt es teilweise zu schweren Verätzungen unter Blasenbildung an Haut und Augen.
Verwendet wird dieses Amin u.a. als Stabilisator, Lösemittel und organischer Säureneutralisator. Außerdem wird es zur Synthese von Kunstharzen, Arzneimitteln und als Schädlingsbekämpfungsmittel genutzt.
Das 1,6-Diaminohexan (Hexamethylendiamin) ist ein wichtiger Rohstoff für die Herstellung von Polyamiden. Durch Polykondensation von 1,6-Diaminohexan mit Hexandisäure erhält man das Polyamid 6,6, das besser unter der Handelsbezeichnung Nylon bekannt ist.
-
Struktur und Eigenschaften von 1,2-Diaminoethan
Das Aminobenzen ist ein aromatisches Amin, das eher unter der Bezeichnung Anilin bekannt ist. Es handelt sich um eine farblose bis rotbraune, ölige Flüssigkeit. In Wasser löst es sich mäßig, in organischen Lösemitteln, wie z. B. Ethanol und Ether, ist es leicht löslich. Das Anilin ist ein starkes Blutgift, da es den Blutfarbstoff (Hämoglobin) und somit die roten Blutkörperchen zerstört. Es ruft Lähmungen hervor und führt bei höheren aufgenommenen Mengen zum Tod durch Herzstillstand. Anilin ist krebserregend.
Anilin ist das wichtigste aromatische Amin und dient als Ausgangsstoff zur Farbenherstellung. Es wird auch für die Produktion von Lösungsmitteln sowie bei der Synthese von Pharmazeutika und Kunststoffen benötigt.
Von Diaminobenzen (Phenylendiamin C6H4(NH2)2) gibt es drei Isomere, die alle die molare Masse von 108,14 g/mol haben. Die Diaminobenzene sind Blutgifte, die den Blutfarbstoff Hämoglobin zerstören und so auch die roten Blutkörperchen. Weiterhin sind Nieren- und auch Leberschäden möglich. Über die Haut und Atemwege können staubförmige Diaminobenzene aufgenommen werden, die zu sehr starken lokalen Reizungen führen können.
Das homologe Diaminotoluen wird in großen Mengen als Diamin-Komponente für die Herstellung von Polyurethanen eingesetzt.
-
Struktur und Eigenschaften von Aminobenzen (Anilin)

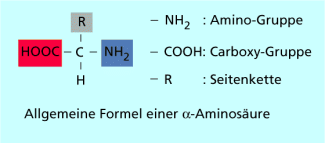
Aminosäuren sind organische Verbindungen mit zwei funktionellen Gruppen, der Amino-Gruppe und der Carboxy-Gruppe (-COOH). Dieser bifunktionelle Charakter führt dazu, dass sie sowohl wie eine Carbonsäure als auch wie ein Amin reagieren können. Deshalb bilden Aminosäuren miteinander Carbonsäureamide, die man Peptide nennt. Sie sind die Grundbausteine der Eiweiße.
Biogene Amine sind Amine, die sich im Organismus aus Aminosäuren bilden. Sie entstehen durch Abspaltung der Carboxy-Gruppe und können wichtige Schlüsselverbindungen in biochemischen Prozessen sein. Biogene Amine spielen z. B. bei der Informationsübertragung im Gehirn als Neurotransmitter eine Rolle. Ihr Aufbau, ihre Entstehung und Erscheinungsformen sind äußerst verschieden und kompliziert.
-
Struktur einer Aminosäure