Chromatografische Analysemethoden – Dünnschichtchromatografie
Die Chromatografie bezeichnet physikalische Trennverfahren, bei denen die Stofftrennung auf der unterschiedlichen Verteilung zwischen einer stationären und einer mobilen Phase, die nicht miteinander mischbar sind, beruht. Bei der Dünnschichtchromatografie erfolgt die Trennung durch mehrstufige Verteilungsprozesse zwischen einer festen stationären Phase und einer mobilen flüssigen Phase hauptsächlich aufgrund von Adsorptions-Desorptions-Wechselwirkungen. Sie findet hauptsächlich zur qualitativen Analyse oder zur Vortrennung von Stoffgemischen Anwendung.
Dünnschichtchromatografie (DC)
Bei der Dünnschichtchromatografie erfolgt die Trennung durch mehrstufige Verteilungsprozesse zwischen einer festen stationären Phase und einer mobilen flüssigen Phase hauptsächlich aufgrund von Adsorptions-Desorptions-Wechselwirkungen.
Adsorption (lat. adsorbere = ansaugen) ist die Anreicherung von Stoffen an den Grenzflächen fester Phasen. Sie unterscheidet sich von der Absorption (lat. absorbere = verschlucken), bei der der Stoff nicht an der Phasengrenzfläche angereichert, sondern in einer flüssigen Phase verteilt wird.
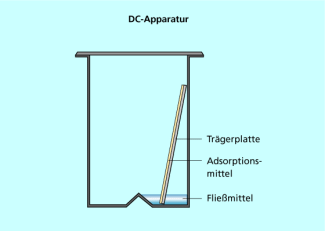
Die stationäre Phase, das Adsorptionsmittel bzw. Sorbens, ist auf einen Träger (Aluminium-, Kunststoff- oder Glasplatte) aufgebracht und wird in die mobile Phase, die hier auch Fließmittel genannt wird, eingetaucht. Als Sorbentien verwendet man am häufigsten Kieselgel, Aluminiumoxid, Cellulose oder Polyamid. Die Proben werden nebeneinander auf die Platten an der Startlinie aufgetragen. Bei manuellem Auftrag können so je nach Plattengröße bis zu 20 Proben parallel analysiert werden. Üblicherweise werden 1 µl oder weniger einer 0,1-1%igen Lösung benötigt. Nach dem Trocknen werden die Platten in die Kammer mit dem Fließmittel gestellt und chromatografiert. Das Fließmittel wird durch Kapillarkräfte entlang der Sorbentienschicht transportiert. Dabei wird die Wanderungsgeschwindigkeit des Analyten um so langsamer, je stärker die Adsorption an der stationären Phase ist (Bild 1).
Die Chromatografie wird abgebrochen, bevor das Fließmittel den oberen Rand der Platte erreicht hat, in der Regel bei 70-80 % der Plattenhöhe.
-
Schematischer Aufbau einer Apparatur für die Dünnschichtchromatografie
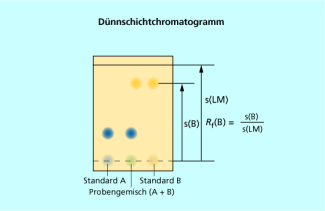
Als Ergebnis der Trennung erhält man auf der Dünnschichtplatte ein Chromatogramm mit mehreren Substanzflecken (Bild 2). Im abgebildeten Chromatogramm hat die Substanz A eine stärkere Wechselwirkung mit der stationären Phase als Substanz B. Sie befindet sich folglich nicht so lange in der mobilen Phase wie Substanz B und wird nicht so weit von ihr transportiert, wandert also nicht so weit wie B.
Das Verhältnis der Wanderungsstrecke der Substanz zur Wanderungsstrecke des Fließmittels wird Rückhaltefaktor oder Retentionsfaktor genannt. Die einzelnen Substanzen A und B lassen sich über den sogenannten identifizieren, wenn dieser mit einer Vergleichssubstanz übereinstimmt.
Er kann nur Werte zwischen 0 und 1 annehmen. Da der von vielen Parametern beeinflusst wird, ist er als stoffspezifische Konstante ungeeignet. Deshalb müssen bei der Dünnschichtchromatografie immer Vergleichssubstanzen zur Identifizierung der Komponenten mit aufgetragen werden.
Da die Anzahl der stationärer Phasen für die DC begrenzt ist, wird in der Regel die Polarität des Fließmittels variiert, um die Auflösung zu verbessern. Zu diesem Zweck setzt man meist Gemische verschiedener Lösungsmittel als mobile Phase ein. Diese Gemische bestehen immer aus verschiedenen Lösungsmitteln die sich in beliebigem Verhältniss mischen lassen, und von denen eines vergleichsweise unpolar und das andere polar ist. Durch Mischen der Lösungsmittel in unterschiedlichem Verhältniss kann man Gemische gleicher Lösungsmittel mit verschiedener Polarität erhalten. Gängige Kombinationen sind z. B. Petrolether oder Hexan als unpolare Komponente und Essigsäureethylester als polare Komponente oder Dichlormethan als unpolare Komponente und Methanol als polare Komponente. Die unzureichende Trennung von 2 Substanzen kann durch Zwischentrocknung und Wechsel des Laufmittels oder durch zweidimensionale Analyse verbessert werden. Dabei wird nach dem ersten Lauf die Platte um 90° gedreht und dann mit einem anderen Laufmittel nochmals chromatografiert. Allerdings kann bei dieser Variante nur ein Gemisch aufgetragen werden und auch das Mitlaufen von Vergleichssubstanzen ist nicht möglich, da es sonst zur Überlagerung kommen würde.
Die Dünnschichtchromatografie erlaubt die Trennung vieler Substanzgemische innerhalb kurzer Zeit mit einem geringen apparativen Aufwand. Mithilfe von UV-Licht oder geeigneten Fluoreszenz- und Sprühreagenzien lässt sich der größte Teil organischer Verbindungen auch sichtbar machen. Sie wird jedoch selten zur quantitativen Analyse eingesetzt, weil die Bestimmung des Anteils der Komponenten A und B aus der Größe der Substanzflecken nicht sehr genau ist.
In der Regel wird die Dünnschichtchromatografie dazu genutzt, um sich einen ersten Überblick über die Zusammensetzung eines Stoffgemisches zu verschaffen. Eine Trennung im größeren Maßstab (präparativ) und quantitative Trennungen werden mit anderen chromtaografischen Methoden wie Säulenchromatografie (LC) bzw. HPLC durchgeführt. Die DC wird hauptsächlich zur qualitativen Analyse von Stoffgemischen verwendet, weiterhin können quantitative Abschätzungen vorgenommen werden. Durch die Einfachheit und den niedrigen Kostenaufwand der Methode wird sie heute hauptsächlich in Laboratorien als Vorstufe zur Säulenchromatografie eingesetzt, um Laufmittel und stationäre Phasen flexibel variieren zu können und schnell Analysenresultate zu erhalten. Durch solche Vorexperimente kann die für ein spezielles analytisches Problem optimale Kombination stationäre/mobile Phase für die HPLC abgeschätzt werden.
Der Vorteil der DC liegt in der gleichzeitigen Analytik mehrerer Proben. Mit moderner automatisierter DC-Technik kann man auf einer DC-Platte 30 bis 40 Proben z. B. von Arzneipflanzen aufbringen und die Wirkstoffzusammensetzung sowie die Gehalte ermitteln. Diese Gerätetechnik erlaubt zudem die Trennung von 20-30 Komponenten auf einer DC-Spur und durch das Abscannen der Substanzflecken mit verschiedenen Wellenlängen sind Möglichkeiten zur Identifizierung und Quantifizierung der Substanzen gegenüber der manuellen Auswertung entscheidend verbessert.
Ein besonderer Fall ist die der Dünnschichtchromatografie eng verwandte Dickschichtchromatografie, die im Gegensatz zu ersterer zum Auftrennen von Stoffgemischen in präparativem Maßstab verwendet wird. Das Prinzip ist das gleiche wie bei der DC. Auf einer größeren Glasplatte (ca. 20 cm x 20 cm) ist eine ca. 0,5 cm dicke Schicht der stationären Phase aufgebracht. In diese können auf der Startlinie bis zu 100 mg des Substanzgemisches aufgebracht werden. Nach der Trennung entsprechend des oben beschriebenen Prinzips wird der größte Teil der Platte abgedeckt und nur ein schmaler Randstreifen z. B. mit dem Nachweisreagenz besprüht. Dann kann man die einzelnen Bereiche der Schicht der stationären Phase, in denen sich die aufgetrennten Substanzen befinden, von der Glasplatte lösen und die Substanzen mit einem geeigneten Lösungsmittel herauswaschen. So ist es z. B. einfach möglich, reines Coffein aus Kaffee oder Tee zu gewinnen.
-
Bestimmung des Retentionsfaktors aus einem Dünnschichtchromatogramm (mit Vergleichssubstanzen)