Chromatografische Analysemethoden – Flüssigkeitschromatografie (LC) und Hochleistungs-Flüssigkeitschromatografie (HPLC)
Die Chromatografie bezeichnet physikalische Trennverfahren, bei denen die Stofftrennung auf der unterschiedlichen Verteilung zwischen einer stationären und einer mobilen Phase, die nicht miteinander mischbar sind, beruht. In der Säulenchromatografie ist die feste stationäre Phase in einem langen, meist senkrecht stehenden Rohr als Säule angeordnet. Das zu trennende Gemisch wird oben auf die Säule gegeben und fließt mit der flüssigen mobilen Phase infolge der Schwerkraft oder angetrieben durch eine Pumpe durch die Säule.
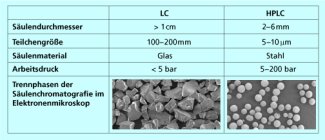
Je nach Säulendurchmesser, Teilchengröße der stationären Phase und Arbeitsdruck unterscheidet man zwischen der klassischen Säulenchromatografie und der modernen Hochleistungsflüssigkeitschromatografie.
Bei der Flüssigkeitschromatografie wird das zu trennende Stoffgemisch mit einer flüssigen mobilen Phase an einer festen Trennphase vorbeigeführt. Die Trennphase kann dabei als plane Schicht aufgebracht sein (z. B. bei der Dünnschichtchromaografie, DC) oder sie befindet sich in einem Rohr bzw. in einer Säule wie bei der LC, IC oder HPLC. Die mobile Phase fließt entweder durch die Schwerkraft an der Festphase vorbei oder sie wird gepumpt.
In Abhängigkeit von der Art der zu analysierenden Stoffe und der dazu benutzten stationären Phase erfolgt die Trennung durch Adsorptions-, Verteilungs- oder Austauschprozesse, die auch durchaus gleichzeitig in einem System ablaufen können.
Je nach Säulendurchmesser, Teilchengröße der stationären Phase und Arbeitsdruck unterscheidet man zwischen der klassischen Flüssigkeitschromatografie (LC), und der modernen Hochleistungs-Flüssigkeits-Chromatografie (high performace liquid chromatography, HPLC).
-
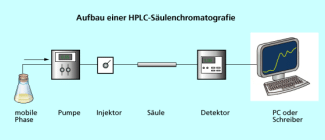
Prinzipieller Aufbau eines HPLC-Säulenchromatografen
Mit der klassischen LC kann man in Abhängigkeit von der Größe der Säule und damit der Menge der stationären Phase Stoffgemische im präparativen Maßstab von einigen Gramm (bis ca. 10 g) trennen.
Bei der HPLC ist die Teilchengröße der stationären Phase deutlich kleiner als bei der klassischen LC. Dadurch wird die zur Verfügung stehende Oberfläche der stationären Phase vergrößert und die Trennleistung der Säule entscheidend verbessert, sodass man mit der HPLC Stoffgemische trennen kann, bei denen die einfache LC versagt. Die kleineren Teilchen sind jedoch so dicht gepackt, dass die mobile Phase mit einer speziellen Pumpe durch die Säule gepumpt werden muss. Infolge dessen passiert die mobile Phase die HPLC-Säule schneller und die Analyse erfolgt in einer viel kürzeren Zeit als bei der klassischen LC (Bild 2).
Der benötigte hohe Druck der HPLC limitiert allerdings die Größe der verwendeten HPLC-Säulen. Die HPLC wird im Allgemeinen hauptsächlich für analytische Zwecke eingesetzt. Mit der sogenannten "präparativen" HPLC können, unter Verwendung von größeren HPLC-Säulen und stärkeren Pumpen, Stoffgemische im präparativen Maßstab von bis zu 100 mg getrennt werden. Damit kann diese Form der HPLC dann nicht nur zur Analyse, sondern ebenso wie die LC auch zur Reinigung / Trennung von Substanzgemischen im chemischen Synthese-Laboratorium verwendet werden.
-
Vergleich von klassischer LC und moderner HPLC-Säulenchromatografie
Die Probe wird über ein spezielles Probenventil in die Mobilphase eingeschleust. Die getrennten Komponenten werden dann nach Verlassen der Säule von einem Detektor beispielsweise über die Absorption im UV-Bereich oder den Brechungsindex erfasst und in einem Signal-Zeit-Diagramm als Chromatogramm dargestellt (Bild 3).
Der qualitative Nachweis wird über die Retentionszeit geführt, die sich aus der Verzögerung ergibt, mit der ein Analyt die Trennstrecke zwischen Injektor und Detektor passiert. Jede Komponente im Analytengemisch hat eine andere Retentionszeit. Sie ergibt sich aus den unterschiedlichen pysikalischen Eigenschaften der Substanzen, wie z. B. ihre Polarität, und die dadurch bedingte unterschiedlich starke Haftung an der Trennphase. Die Identifizierung erfolgt wie bei den anderen chromatografischen Verfahren mittels Testssubstanzen und Vergleich der Retentionszeiten oder durch die Verwendung eines Massenspektrometers als „intelligentem“ Detektor. Die Konzentration der Analyten wird aus der Fläche unter dem Peak berechnet. Je größer der Anteil der Komponente in der Probe, desto größer wird der Peak. Um die quantitative Bestimmung so genau wie möglich zu führen, kalibriert man die Methode mit Standards bekannter Zusammensetzung.
Auf diese Weise kann man speziell mit der HPLC eine sehr genaue und zuverlässige quantitative Analyse durchführen, die automatisierbar und für viele analytische Zwecke einsetzbar ist.
Mithilfe der HPLC können Spuren von Dioxinen in Bodenproben oder sogar in Lebensmitteln nachgewiesen werden. Dafür ist aber eine aufwendige Abtrennung störender Substanzen und eine Aufkonzentrierung erforderlich. Die Konzentration von Dopingmitteln wie Erythropoietin (EPO) im Blut von Sportlern wird ebenfalls mittels HPLC bestimmt. Die Methode findet auch in der Arzneistoffanalytik viele Anwendungen.
So kann z. B. die Alterung von Aspirin® untersucht werden, indem man das Verhältnis von Acetylsalicylsäure und der Salicylsäure chromatografisch analysiert. Auch andere Verunreinigungen und Abbauprodukte des Präparats werden auf diese Weise zuverlässig nachgewiesen.
Eine besondere Ausführungsform der HPLC ist die Ionenchromatografie (IC) zur Trennung von Ionen in wässriger Lösung. Sie basiert auf dem Trennmechanismus des Ionenaustausches und wird für die Trennung von anorganischen Anionen und Kationen herangezogen. Die Grundlage für die Trennung bildet ein Ionenaustauschprozess. Dieser findet zwischen den in der mobilen wässrigen Phase gelösten Ionen und den am Trägermaterial gebundenen Ionen an den Austauschergruppen als stationärer Phase während des Durchlaufs der Lösung durch eine Trennsäule statt. Die stationäre Phase der Trennsäule besteht z. B. aus einem Polystyrol-Divinylbenzol-Harz, das zur Trennung der Anionen fest verankerte kationische Austauschergruppen (z. B. –NR3 +) und austauschbare Gegenionen des Eluenten (z. B. HCO3 -) besitzt. An Harzen mit anionischen Austauschergruppe wie –SO3 - H+ können Kationen ausgetauscht werden.
Die getrennten Ionen werden dann mit einem Detektor durch Messung der elektrischen Leitfähigkeit registriert.
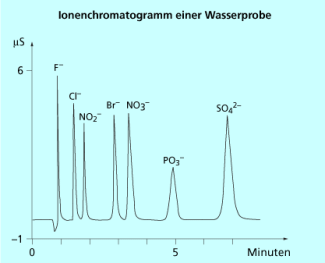
Die Ionenchromatografie zeichnet sich dadurch aus, dass die Messung relativ schnell bei hoher Empfindlichkeit und Selektivität erfolgt. Die Trennsäulen sind langzeitstabil. Aus diesen Gründen ist die Umweltanalytik eines der Hauptanwendungsgebiete der Ionenchromatografie. Hier wird die Ionenchromatografie zur qualitativen und quantitativen Analyse von Anionen und Kationen in Gewässer-, Boden- oder Luftproben genutzt. So ist es beispielsweise möglich, die Anionen Fluorid, Chlorid, Nitrit, Bromid, Nitrat, Phosphat und Sulfat, die die Qualität eines Wassers maßgeblich beeinflussen, in wenigen Minuten zu trennen und zu bestimmen (Bild 5). Auch in der Lebensmittelindustrie findet diese Methode breite Anwendung, so beispielsweise zur Analyse der verschiedenen Fruchtsäuren in Saft oder Wein.
-
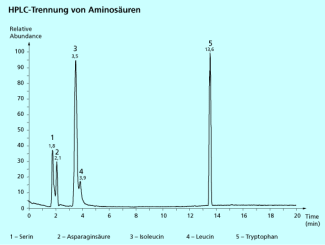
Trennung von Aminosäuren mittels HPLC
-
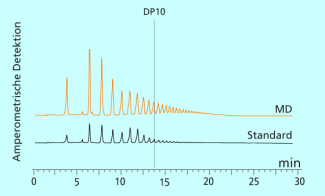
Auftrennung eines Oligosaccharidgemischs mittels HPLC und Vergleich der Probe mit einem Standard definierter Kettenlänge (jeder Peak entspricht dabei einer weiteren Glucoseeinheit; der allererste Peak ist ein Salzpeak).
-
Ionenchromatogramm einer Wasserprobe Konzentrationen jeweils etwa 10 mg l-1)