Fotosynthesepigmente
Fotosynthesepigmente sind Pigmente, die Licht absorbieren und mithilfe der Lichtenergie von einem energiearmen Grundzustand in einen energiereichen, angeregten Zustand übergehen. Beim Zurücksprung in den Grundzustand - der angeregte Zustand ist zwar energievoll aber instabil - wird die Energie in Form von Photonen an ein bestimmtes Chlorophyll-a-Molekül, ebenfalls ein Fotosynthesepigment, abgegeben, dass sich in einem Reaktionszentrum befindet. Mithilfe dieser Energie findet dann die erste lichtbetriebene, chemische Reaktion statt, eine Redoxreaktion.Diejenigen Pigmente, die das Licht absorbieren und dessen Energie bis zu den Pigmenten im Reaktionszentrum weiterleiten, heißen Antennenpigmente. Antennenpigmente sind verschiedene Chlorophyll-Protein-Komplexe, Carotinoide und Phycobiline. Jedes fotosynthetische Reaktionszentrumschlorophyll ist von etwa 300 verschiedenen, lichtsammelnden Antennenpigmenten umgeben.
Die gesamte Struktur, Antennenpigmente und Reaktionszentrum, wird Fotosystem genannt.
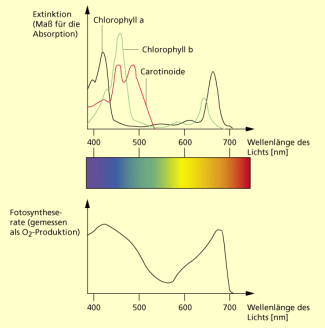
Der deutsche Botaniker THEODOR WILHELM ENGELMANN (1843 – 1909) konnte 1883 mit seinen Versuchen mit einer fadenförmigen Alge die Fotosyntheseaktivität in den verschiedenen Bereichen des sichtbaren Lichtes nachweisen. Diese entspricht im Wesentlichen den Absorptionsmaxima der Fotosynthesepigmente bzw. dem Zusammenwirken der Farbstoffe im Fotosystem. Chlorophylle stellen die Hauptpigmente in allen fotoautotrophen Organismen dar. Carotinoide und Chlorophylle sind vorwiegend als Antennenpigmente zur optimalen Lichtabsorption im Rahmen des Antennenkomplexes im Fotosystem vertreten.
Der deutsche Physiologe THEODOR WILHELM ENGELMANN beleuchtete 1883 eine fadenförmige Alge (Oedogonium) und ermittelte so zum ersten Mal das Wirkungsspektrum der Fotosynthese. Bei dem Experiment schickte er weißes Licht durch ein Prisma, wodurch das Licht in die verschiedenen Wellenlängen aufgetrennt wurde und so die Alge in verschiedenen Bereichen bestrahlte. Zugesetzte Sauerstoff liebende (aerophile) Bakterien zeigten ENGELMANN durch ihre plötzliche Aktivität an, in welchen Wellenlängen des sichtbaren Lichtes am meisten Sauerstoff hergestellt worden und so die Fotosyntheseaktivität am größten ist. Die im Experiment ermittelten vorwiegend roten und blauen Bereiche des sichtbaren Lichtes entsprechen dem Wirkungsspektrum der Fotosynthese und den möglichen Absorptionsmaxima der Fotosynthesepigmente bei den eingesetzten Algen.
Fotosynthesepigmente werden für die Lichtabsorption und die damit verbundene Umwandlung der Lichtenergie in chemische Energie im Rahmen der Fotosynthese benötigt. Diese Farbstoffe sind in den Thylakoidmembranen (Stroma- und Granathylakoide) der Chloroplasten eingelagert und bilden ein sogenanntes Fotosystem, welches aus Reaktionszentrum und Antennenkomplex (LHC: Light Harvesting Complex) besteht. Durch Chromatografie (Trennverfahren) kann man die einzelnen Fotosynthesepigmente auftrennen. Es lassen sich die Farbstoffe Chlorophylle, Carotinoide und Phycobiliproteide isolieren.
-
Spektrum der Fotosynthese
Chlorophylle
Chlorophylle (Blattgrün) sind die grünen Farbstoffe der grünen Pflanzen, fotosynthetisierender Algen und bestimmter Bakterien und stellen in allen fotoautotrophen Organismen das wichtigste absorbierende Pigment für die Fotosynthese dar.
Durch die Absorption der Lichtenergie der Sonne wird im Rahmen der Fotosynthese die chemische und für Stoffwechselreaktionen allgemein verwertbare Energie von ATP (Adenosintriphosphat) in die Reduktionsäquivalente NADPH (Nicotinamidadenindinucleotidphosphat) umgewandelt. Bei Höheren Pflanzen sind Chlorophylle in der inneren Membran (Thylakoidmembran) der Chloroplasten lokalisiert. Die Befestigung in der Membran erfolgt durch den lipophilen Phytol-Rest.
-
Chlorophyll a und Chlorophyll b
1918 bestimmten RICHARD WILLSTÄTTER (13.08.1872 – 03.08.1942) und ARTHUR STOLL (8.1.1887-13.1.1971) die Struktur des Chlorophylls, nachdem sie 1913 die Ähnlichkeit zu Hämoglobin nachwiesen.
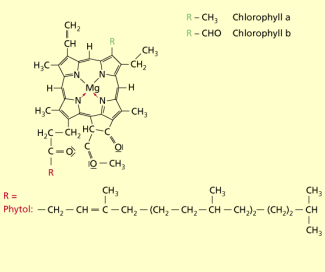
Chlorophylle bestehen aus einem Porphyrinring, der durch 4 über Methin-Brücken miteinander verknüpfte Pyrrolringe gebildet wird sowie Magnesium als Zentralatom. Durch ihre Ableitung vom Porphyringerüst besteht eine strukturelle Verwandtschaft mit dem Häm der Hämoglobine, Myoglobine und Cytochrome. Die weisen jedoch ein zweiwertiges Eisenion als Zentralatom auf.
Die einzelnen Chlorophylle unterscheiden sich durch Abwandlungen der Seitengruppen des Ringgerüsts, d. h. verschiedene Reste an den Pyrrolringen (Substitutionsmuster) und die Art der alkoholischen Isoprenseitenkette (z. B. Phytol). Man unterscheidet Chlorophylle a, b, c, d und e. Die Hauptrolle bei allen zur Fotosynthese befähigten Organismen spielt das Chlorophyll a. Bei höheren Pflanzen und einigen Algen ist zusätzlich das Chlorophyll b verbreitet (ca. 1/3 der Konzentration von Chlorophyll a). Die anderen Chlorophyllarten sind bei einzelnen Organismengruppen anzutreffen, so z. B. Chlorophyll c bei Braunalgen, welches durch einen anderen chemischen Aufbau im Vergleich zu Chlorophyll a und b wasserlöslich ist.
Bei Chlorophyll a und b ist die Propionseitenkette des Pyrrolringes D mit einem langkettigen Alkohol aus 20 Kohlenstoffatomen verestert (Phytol). Dieser chemische Aufbau ist für die Lipidlöslichkeit der beiden Chlorophylle und die Verankerung in der Thylakoidmembran verantwortlich. Chlorophyll b unterscheidet sich lediglich durch eine Formyl- statt einer Methylgruppe am Pyrrolring B vom Chlorophyll a. Diese Veränderung im chemischen Aufbau hat eine Auswirkung auf die Farbe von Chlorophyll a (blaugrün) und Chlorophyll b (gelbgrün) sowie auf die Lage der Absorptionsmaxima der beiden Chlorophyllarten. Beide absorbieren vorwiegend Licht im blauen und roten Bereich des sichtbaren Lichtes, wobei die mittleren Wellenlängen von den Chlorophyllen a und b nicht abgedeckt werden („Grünlücke“). Chlorophyll b hat im Vergleich zum Chlorophyll a leicht versetzte Absorptionsmaxima und verkleinert so die „Grünlücke“. Deswegen kommt Chlorophyll b als Antennenpigment (= akzessorisches Pigment) im Antennenkomplex vor. Hier zeigt sich, dass die Absorption des Sonnenlichtes durch die Chlorophylle und die damit verbundene Bereitstellung für fotochemische Arbeit nicht optimal sind.
Einige spezielle Eigenschaften der Chlorophylle sorgten aber im Laufe der Evolution dafür, dass sie sich als Hauptpigment für die Fotosynthese durchgesetzt haben:
| Chlorophylle können die absorbierte Lichtenergie auf andere Moleküle übertragen und von anderen Molekülen aufnehmen. Dabei besitzen die Empfänger eine höhere Wellenlänge als die Spendermoleküle und wirken so in ihrer Gesamtheit als Licht- bzw. Energiefalle. | |
| Sie besitzen in ihrem chemischen Aufbau eine große Anzahl an konjugierten Doppelbindungen, d. h. es sind viele bewegliche Elektronen vorhanden, die sich durch einen geringen Energieaufwand auf ein höheres Energieniveau bringen lassen. | |
| Besondere Chlorophyll a Moleküle, deren Absorptionsmaxima bei 700 nm bzw. 680 nm liegen („P 700“, „P 680“), besitzen als Reaktionszentren der beiden Fotosysteme die Möglichkeit, bei Belichtung vorübergehend Elektronen auf ein höheres Energieniveau abzugeben. Diese Fähigkeit ist für den Elektronentransport bei den lichtabhängigen Reaktionen und somit für den gesamten Ablauf der Fotosynthese entscheidend. |
Fotoautotrophe Bakterien besitzen ebenfalls Chlorophylle, die sich in ihrem chemischen Aufbau nur gering von den Chlorophyllen der Eukaryoten unterscheiden und als Bacteriochlorophylle bezeichnet werden. Es sind die Bacteriochlorophylle a bis d bekannt. Sie unterscheiden sich von den Chlorophyllen der Eukaryoten durch die Reduktion eines Pyrrolringes und die Veresterung mit Farnesol (Alkohol mit 15 Kohlenstoffatomen) statt mit Phytol (Ausnahme Bacteriochlorophyll a). Dadurch sind die fotoautotrophen Bakterien in der Lage sehr langwelliges Rot zu absorbieren (z. T. bis 900 nm), welches für Ablauf und Effektivität der Fotosynthese bei den Bakterien in ihren Lebensräumen vorteilhaft ist.
Carotinoide
Carotinoide, die wegen ihrer Fettlöslichkeit auch Lipochrome genannt werden, sind lipophile Farbstoffe, die durch eine gelbe, orange oder rote Farbe gekennzeichnet sind. Die Farbigkeit beruht auf dem System mehrerer konjugierter Doppelbindungen, welche je nach Anzahl und Lage das Licht bestimmter Wellenlängen absorbieren (bis über 500 nm, blauer Bereich des sichtbaren Lichts). Carotinoide kommen nicht nur bei autotrophen Organismen sondern auch bei Tieren und Menschen vor, wobei diese alle aus pflanzlicher Nahrung in den Organismus gelangen, so z. B. in Gefieder, Auge, Milch oder Eidotter. Auch die rote Farbe eines gekochten Hummers ist auf das Carotinoid Astaxanthin zurückzuführen. Alle stammen aber aus pflanzlicher Nahrung, da Carotinoide nur von Pflanzen innerhalb der Chloro- oder Chromoplasten (Plastiden) gebildet werden können.
Die Carotinoide Höherer Pflanzen kommen in Laubblättern, Früchten, Sprossachsen, Wurzeln, Staubblättern, Pollen und Samen vor. Die Farbe der Carotinoide in den Chloroplastenmembranen grüner Laubblätter tritt auffällig im Herbstlaub hervor, wenn beim Welken der Laubblätter das Chlorophyll abgebaut wird und die Chloroplasten in Chromoplasten umgewandelt werden. Ähnliches passiert bei der Reifung von grünen zu farbigen Früchten. Beispiele für Carotinoide in Früchten sind
- Lycopin (in Tomate, Hagebutte, Rose)
- Capsanthin (in rotem Pfeffer) und
- Capsorubin (in Paprika).
Bei großer Anreicherung von Carotinoiden liegen sie nicht mehr als Lipidtropfen an die Membran gebunden vor, sondern werden als Kristalle ins Cytoplasma ausgestoßen. So gelangen sie auch in pflanzliches Speichergewebe, wie beispielsweise bei der Möhre. Vereinzelt kommen Carotinoide auch als Blütenfarbstoff vor (z. B. Krokus, Veilchen, Stiefmütterchen). Eine Ausnahme ist das Vorkommen in Samen beim Maissamen.
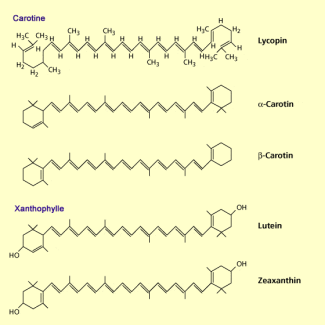
Carotinoide besitzen meistens 40 Kohlenstoffatome mit stark konjugierten Doppelbindungen. Die 40 Kohlenstoffatome bestehen oft aus zwei symmetrischen Einheiten zu je 20 Kohlenstoffatomen. Carotinoide lassen sich in Carotine und Xanthophylle einteilen.
Carotine sind reine Kohlenwasserstoffe mit oranger bis roter Farbe und weisen keinen Sauerstoff auf. Das bekannteste Carotin ist das ß-Carotin (Pro-Vitamin A), welches bei Pflanzen, Algen und Cyanobakterien vorkommt. Durch die Halbierung des Moleküls und der Anlagerung einer Hydroxylgruppe entstehen aus dem ß-Carotin zwei Moleküle Vitamin A.
Xanthophylle sind sauerstoffhaltige Derivate der Carotine. So kommt z. B. Lutein bei Pflanzen und Grünalgen vor. Fucoxanthin ist dagegen bei Braunalgen isoliert worden.
Carotinoide absorbieren im blauen Bereich (Wellenlänge über 500 nm) des sichtbaren Lichtes, also in den Wellenlängen, wo Chlorophylle eine geringe Absorption aufweisen (Verkleinerung der Grünlücke). Sie kommen daher in den Fotosystemen als Antennenpigmente im Antennenkomplex vor (LHC). Allerdings wurde in den letzten Jahren festgestellt, dass sie die Lichtenergie nur mit einer geringen Effektivität auf andere Pigmente übertragen. Carotinoide schützen aber zusätzlich Membranbestandteile vor Angriffen des molekularen Sauerstoffs (fotooxidative Zerstörung) und ist somit für die Funktion der Fotosysteme von Bedeutung.
In Blütenblättern und Früchten sind Carotinoide als Lockfarben für Tiere von Bedeutung. Wichtig auch die Funktion einiger Carotinoide als Provitamin (Carotin). Heute vielfach auch künstlich hergestellte Carotinoide werden in Medikamenten als Vitamin-A-Vorstufen, als Nahrungsmittelfarbstoffe (Käse, Fruchtsäfte) und als Futtermittelzusatz verwendet.
-
Carotinoide
Phycobiliproteine
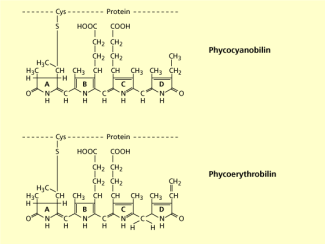
Diese Fotosynthesepigmente kommen vor allem bei Cyanobakterien und Rotalgen vor. In unterschiedlichen Mischungsverhältnissen von Phycocyanen (blau) und Phycoerythrinen (rot) überdecken sie die Chlorophylle und geben so den genannten Organismen die charakteristische Farbe. Wie aus dem Namen abzuleiten ist, bestehen diese wasserlöslichen Farbstoffe aus einem Proteinanteil und den Farbstoffen Phycocyanobilin bzw. Phycoerythrobilin. Das sind offenkettige Tetrapyrrole, ähnlich den Gallenfarbstoffen, die durch den Abbau von Hämoglobin entstehen.
Phycobiliproteine kommen als Bestandteile der Antennenpigmente an der Thylakoidoberfläche vor und bilden in ihrer Gesamtheit sogenannte Phycobilisomen (z. B. bei Rotalgen). Ihre Absorptionsleistungen sind vom chemischen Aufbau abhängig (Tetrapyrrolanteil, Bindung und Bau des Proteins). Sie absorbieren Lichtenergie in dem Bereich, wo Chlorophylle und Carotinoide nur geringe Absorptionsleistungen haben und verkleinern so die Grünlücke noch weiter. So können z. B. Rotalgen auch noch in sehr großen Wassertiefen vorkommen und Fotosynthese betreiben. Bemerkenswert ist dabei, dass sie meist einen direkten Kontakt zu Chlorophyll a Molekülen haben und die Energieübertragung mit rund 95% sehr effektiv ist.
Im Bereich des grünen Lichts absorbieren Fotosynthesepigmente kaum. Deshalb sehen die Blätter grün aus.
-
Phycobiliproteide b