Lösungsmittel und ihre Eigenschaften
Lösungsmittel sind flüssige Verbindungen, die feste, flüssige und gasförmige Substanzen lösen können, ohne diese oder sich selbst chemisch zu verändern. Bei einem Lösevorgang wird die Gitterenergie der Verbindung aufgehoben. Dabei werden energetisch weniger fest gebundene äußere Kristallmoleküle oder -ionen einer Verbindung durch das Lösungsmittel herausgelöst, in Form einer Hülle abgefangen und stabilisiert. Ebenso müssen die inneren Kräfte der Lösungsmittelmoleküle überwunden werden. Die benötigte Energie wird aus der Anziehung zwischen den gelösten Teilchen und dem Lösungsmittel erhalten. Im Fall von Wasser bezeichnet man diesen Vorgang als Hydratisierung, bei anderen Lösungsmitteln von Solvatisierung. Neben Wasser, das sich durch seine Fähigkeit zur dreidimen sionalen Ausbildung von Wasserstoffbrücken auszeichnet, werden viele anorganische und organische Flüssigkeiten als Lösungsmittel eingesetzt. Sie gehören zu den nichtwässrigen Systemen und werden nach ihrer Fähigkeit zur Abgabe von Protonen oder anderen Ionen und ihrer Polarität in die Kategorien protisch, aprotisch unpolar und aprotisch polar unterteilt.
, d. h. lösen können (Bild 1). Stoffe können in unterschiedlichen Konzentrationen in einer Lösung vorliegen. Dementsprechend unterscheidet man zwischen konzentrierten, verdünnten, ungesättigten, gesättigten und übersättigten Lösungen. Dabei liegt stets eine Gleichgewichtsreaktion zwischen der zu lösenden Verbindung und dem Lösungsmittel auf der einen Seite und der Lösung auf der anderen Seite vor. Bei gesättigten Lösungen liegt ein Gleichgewicht zwischen den in Lösung gehenden und ausfallenden Teilchen vor (Löslichkeitsprodukt).
Das Lösungsmittel ist stets im Überschuss vorhanden und sollte weder sich noch den gelösten Stoff chemisch verändern. Die entstehenden Lösungen sind homogene Mischungen von zwei oder mehr Stoffen, die in Abhängigkeit von der Teilchengröße der gelösten Stoffe in echte und kolloide Lösungen eingeteilt werden. In beiden Fällen sind die aufgelösten Teilchen weder mit bloßem Auge erkennbar noch durch ein Papierfilter abfangbar.
Lösungsmittel können neben Wasser auch organische oder anorganische Stoffe sein, die flüssig sind. Grundsätzlich gilt die Regel, dass unpolare Lösungsmittel unpolare Stoffe und polare Lösungsmittel polare Stoffe und Ionen lösen. Der Vorgang des Lösens besteht in der Überwindung der Gitterenergie. Äußere Kristallmoleküle oder Ionen eines Stoffes, die durch geringere Energie gebunden sind, werden aus dem Verband herausgelöst und von Lösungsmittelmolekülen durch elektrostatische Wechselwirkungen solvatisiert und dadurch stabilisiert.
Wirkung
Zudem müssen auch die Kräfte innerhalb der Lösungsmittelmoleküle überwunden werden. Die dafür benötigte Energie wird aus der Anziehung zwischen dem Lösungsmittel und der gelösten Verbindung erhalten. Im Fall der Beteiligung von Wasser (wässrige Systeme) spricht man von einer Hydratisierung, bei allen anderen Lösungsmitteln (nichtwässrige Systeme) von einer Solvatisierung. Zur Optimierung des Reaktionsverlaufes, aber auch aus wirtschaftlichen Gründen, werden häufig Lösungsmittelgemische eingesetzt.
Das Lösungsmittel geht eine Säure-Base-Reaktion ein. Wasser und Ammoniak sind Beispiele für die Autoprotolyse:
Autoprotolyse von Wasser
Autoprotolyse von Ammoniak
Andere Lösungsmittel tauschen entweder analog Protonen oder andere Ionen aus. Unabhängig von der Art des Lösungsmittels steigt die Löslichkeit von festen und flüssigen Verbindungen häufig, aber bei weitem nicht immer bei einem Temperaturanstieg, die von Gasen sinkt.
-
NaCl in Wasser gelöst
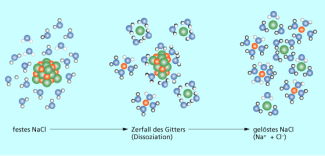
Wasser
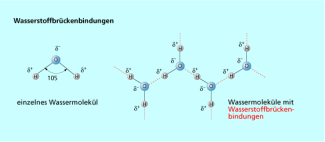
Wasser zeichnet sich durch seine Fähigkeit zur dreidimensionalen Wasserstoffbrückenbindung aus, weil Wechselwirkungen zwischen dem elektronegativen Sauerstoff mit seinen freien Elektronenpaaren und den Protonen vorliegen (Bild 2). Damit ein Stoff in Wasser gelöst werden kann, müssen Wasserstoffbrücken aufbrechen und die elektrostatischen Kräfte im zu lösenden Stoff überwunden werden. In Wasser lassen sich deshalb Salze, Säuren, Basen und organische Verbindungen mit Wasser liebenden (hydrophilen) Gruppen z. B. -OH, -CO2H, -SO3H, -NH2 und NH4 +) gut lösen.
Anorganische und organische Lösungsmittel
Sowohl bei anorganischen als auch bei organischen Lösungsmitteln wird zwischen protischen, polar aprotischen und unpolar aprotischen Lösungsmitteln unterschieden. Protische Lösungsmittel können wie Wasser Protonen zur Verfügung stellen, während aprotische Lösungsmittel keine positiv polarisierbaren Wasserstoffatome besitzen. Polar aprotische Lösungsmittel haben ebenso wie protische eine hohe Dielektrizitätskonstante, weil sich stark elektronegative Atome oder funktionellen Gruppen in ihren Molekülen befinden und die Ladungen nicht gleichmäßig verteilt sind.
Anorganische Lösungsmittel sind beispielsweise Wasser ![]() , flüssiger Ammoniak und Schwefeldioxid flüssiger Florwasserstoff (HF), Thionyl- (SOCl2) und Sulfonylchlorid (SO2Cl2) sowie Schwefelsäure
, flüssiger Ammoniak und Schwefeldioxid flüssiger Florwasserstoff (HF), Thionyl- (SOCl2) und Sulfonylchlorid (SO2Cl2) sowie Schwefelsäure
Zu den typischen organischen Lösungsmittel zählen Alkohole (Methanol), Carbonsäureester (Ethylacetat), Ether (Diethylether), Ketone (Aceton), Alkane (n-Hexan), aromatische Kohlenwasserstoffe (Toluol), halogenierte aliphatische Kohlenwasserstoffe (Tetrachlorkohlenstoff) und Glykolether (Ethylenglykolmonoethylether).
| Protische Lösungsmittel | ||
Klasse | Beispiele | Formel |
| Wasser | ||
| Alkohole | Methanol, Ethanol | |
| Carbonsäuren | Ameisensäure | |
| Aprotische Lösungsmittel | ||
Klasse | Beispiele | Formel |
| unpolar | ||
| Alkane | n-Pentan | |
| Aromatische KW | Toluol | |
| Halogenalkane | Tetrachlorkohlenstoff | |
| Ether | Diethylether | |
| polar | ||
| Ketone | Aceton | |
| Nitrile | Acetonitril | |
Dimethylsulfoxid und Dimethylformamid gehören auch zu der Klasse der aprotischen polaren Lösungsmittel.
Durch die Wahl eines entsprechenden Lösungsmittels können der Reaktionsmechanismus, der zeitliche Ablauf einer Reaktion und die Ausbeute gesteuert werden.
Wie groß der Einfluss eines Lösungsmittels sein kann, erkennt man bei der nucleophilen Substitution. Nucleophile Substitutionen müssen als polare Reaktionen in einem Lösungsmittel ablaufen, um die Zwischenstufen durch Solvatisierung zu stabilisieren. Der geschwindigkeitsbestimmende Schritt einer ist die Bildung eines Carbenium-Ions /Ionenpaares. Stark polar protische Lösungsmittel wie Carbonsäuren oder auch Ammoniak vermögen durch ihre freien Elektronenpaare das Kation zu stabilisieren und durch ihre Protonen das Anion (Abgangsgruppe) aus dem Molekül zu drängen. Besonders wirksam sind auch Alkohol/ Wassergemische, wobei dann aber die Gefahr besteht, dass nicht nur das entsprechende Nucleophil das Carbenium-Ion angreift, sondern letzteres mit dem Wasser eine Hydrolyse eingeht. Das liegt daran, dass dieses Lösungsmittelgemisch in seiner dissoziierten Form reaktiver sein kann als die in der Lösung vorliegenden Reagenzien. Damit kann ein Lösungsmittel auch Einfluss auf den Reaktionsmechanismus, den zeitlichen Ablauf und/oder auf die Ausbeute nehmen.
Im Fall einer eignen sich dagegen polar aprotische Lösungsmittel wie Dimethylformamid, Aceton oder Ether, die keine positiv polarisierten Wasserstoffatome besitzen. Bedeutend ist hier, dass während der Bildung des aktivierten Komplexes, in dem das Nucleophil angreift und die Abgangsgruppe austritt, keine ausgeprägte Solvathülle die Vorgänge behindert.
In Abhängigkeit von der Struktur der Abgangsgruppe und der Stärke bzw. der Schwäche des Nucleophils kann durch den Einsatz verschiedener Lösungsmittel oder Lösungsmittelgemische sogar eine Steuerung zu einer erfolgen.
-
Wasserstoffbrückenbindung
Nach beendeter Reaktion muss das Lösungsmittel vom Reaktionsprodukt abgetrennt werden. Das geschieht häufig durch Destillation (Bild 3). Das Lösungsmittel wird somit zurückgewonnen und kann erneut eingesetzt werden. Dabei ist aber zu beachten, dass sich bei mehrfacher Nutzung des Lösungsmittels Verunreinigungen darin anreichern können. Diese Verunreinigungen waren beispielsweise in den Ausgangsstoffen enthalten oder sind durch Nebenreaktionen entstanden und können nun Störungen verursachen.
Die meisten Lösungsmittel sind gesundheitsschädlich, weil sie leicht verdunsten und lipophile Eigenschaften besitzen. Sie können durch die Poren der Haut und durch ungeschützte Atmung in den menschlichen Organismus gelangen. Deshalb müssen sowohl für den Umgang als auch für die Entsorgung unbedingt die gesetzlich vorgeschriebenen Sicherheitsbestimmungen eingehalten werden.
Suche nach passenden Schlagwörtern
- anorganische Stoffe
- Nucleophile Substitution
- kolloide Lösungen
- polare aprotische Lösungsmittel
- polare Lösungsmittel
- protische Lösungsmittel
- anorganische Lösungsmittel
- Solvatisierung
- Teilchengröße
- Hydratisierung
- homogene Mischungen
- unpolare Lösungsmittel
- organische Stoffe
- Autoprotolyse
- organischen Lösungsmitteln
- echte Lösungen
- aprotische Lösungsmittel
- Wasser
- Lösungsmittel
- Wasserstoffbrückenbindung

