Prinzip des kleinsten Zwangs (Prinzip von LE CHATELIER)
Chemische Gleichgewichte lassen sich nicht nur durch Änderung der Konzentrationen, der Ausgangsstoffe oder Produkte beeinflussen, sondern auch durch äußere Einflüsse, wie z. B. Temperatur- und Druckveränderungen. Hier gilt stets das von LE CHATELIER und K. F. BRAUN formulierte Prinzip des kleinsten Zwangs. Dieses besagt, dass sich das chemische Gleichgewicht einem äußeren Zwang immer so entzieht, dass die Wirkungen der äußeren Veränderung verkleinert werden.
Das Prinzip des kleinsten Zwangs, auch benannt als Prinzip von LE CHATELIER nach dem gleichnamigen Chemiker, wurde 20 Jahre nach der Entdeckung des Massenwirkungsgesetzes 1887 bekannt.
HENRY LOUIS LE CHÂTELIER (1850-1936) war Professor für Chemie in Paris. Seine Hauptarbeitsgebiete waren die spezifische Wärme von Gasen, die Silicatchemie und auch das chemische Gleichgewicht.
KARL FERDINAND BRAUN (1850-1918) war Professor für Physik in Straßburg. Er arbeitete unter anderem mit elektromagnetischen Wellen, entwickelte die Bsche Röhre und befasste sich ebenfalls mit dem chemischen Gleichgewicht.
Beide Naturwissenschaftler untersuchten unabhängig voneinander die Beeinflussung chemischer Gleichgewichte durch Temperatur- und Druckveränderungen. Die von ihnen erkannten Gesetzmäßigkeiten werden heute in der Chemie kurz unter dem Prinzip des kleinsten Zwanges zusammengefasst.
Dieses besagt:
| Übt man auf ein im Gleichgewicht befindliches stoffliches System einen Zwang aus, so verschiebt sich das Gleichgewicht so, dass das System dem äußeren Zwang ausweicht, wobei dessen Wirkungen verringert werden. |
Dieses Prinzip berücksichtigt die qualitativen Wirkungen von Druck- und Temperaturveränderungen auf physikalische (z. B. Kondensieren und Verdampfen) und chemische Gleichgewichte.
Das Prinzip von LE CHATELIER und BRAUN beschreibt also nicht die Abhängigkeit des chemischen Gleichgewichts von stofflichen Faktoren, z. B. die Konzentrationen der Ausgangsstoffe oder Produkte, sondern die von äußeren Bedingungen.
Äußere Zwänge können Temperatur- oder Druckveränderungen sein.
Einfacher zu erklären sind die Folgen einer Druckveränderung auf ein Gleichgewichtssystem. Obwohl man mit Druck primär nur jene Gleichgewichte beeinflussen kann, bei denen eine Volumenänderung stattfindet, sind streng genommen alle chemischen Gleichgewichte druckabhängig. Das liegt daran, dass bei der Umsetzung der Ausgangsstoffe Reaktionsprodukte mit anderen Dichten entstehen. Und so verändert sich stets auch das Volumen eines Systems, wenn auch nur sehr wenig, da die Gesamtmasse des Systems konstant bleibt (Gesetz von der Erhaltung der Masse).
Beeinflussung durch den Druck
Der Druck hat nur merklichen Einfluss auf chemische Gleichgewichtsreaktionen, wenn Gase beteiligt sind und sich die Volumina der Ausgangsstoffe von den Volumina der Reaktionsprodukte unterscheiden.
Druckerhöhung fördert die Reaktion, die unter Volumenabnahme verläuft. Druckerniedrigung fördert die Reaktion, die unter Volumenzunahme verläuft.
Beispiel: Ammoniaksynthese (siehe HABER-BOSCH-Verfahren)
Die Bildung von Ammoniak verläuft im Vergleich zu den Volumina der Ausgangsstoffe unter Volumenverringerung (siehe Bild 1).
Das Gleichgewicht lässt sich unter Druck auf die Seite des Ammoniaks verschieben.
Das Prinzip des kleinsten Zwanges lässt sich damit begründen, dass das System dem erhöhten Druck ausweicht, indem es sich auf die Seite der volumenärmeren Produkte verschiebt. Es wirkt dem äußeren Einfluss entgegen, indem es die Anzahl der Moleküle in der Gasphase verringert.
Um die Rückreaktion, die Zersetzung von Ammoniak, zu begünstigen, müsste man den Druck verringern.
Beeinflussung durch die Temperatur
Grundsätzlich gilt: Ist der äußere Zwang durch eine Temperaturerhöhung gekennzeichnet, verschiebt sich das Gleichgewicht zugunsten einer endothermen Reaktion, so dass mehr Wärme vom System aufgenommen wird.
Bei Temperaturverringerung läuft bevorzugt die exotherme Reaktion ab. Das stoffliche System weicht bei einer Temperaturerniedrigung solange aus, bis sich das Gleichgewicht neu eingestellt hat.
Es gilt wieder das Prinzip des kleinsten Zwanges, da sich das System der Veränderung entzieht, indem es die Folgen des Zwanges verkleinert.
Beispiel:
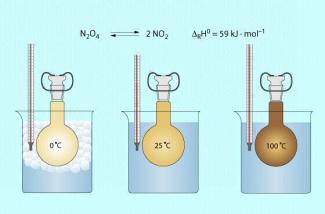
Das Stickstoffdioxid hat eine braune Farbe, das Distickstofftetraoxid ist farblos. Die Reaktion ist bei Zimmertemperatur exotherm.
Erhöht man die Temperatur des Systems, wird sich die Farbe des Gasgemisches stärker braun färben, da sich mehr Stickstoffdioxid bildet (Bild 1).
Die endotherme Reaktion (hier: Zersetzung von Distickstofftetraoxid) findet statt. Das System entzieht sich dem Zwang, indem es die Energie der Temperaturerhöhung zum Zersetzen von Distickstofftetraoxid verwendet.
Umgekehrt wird sich das Gasgemisch bei Temperaturerniedrigung langsam entfärben. Es wird der Erniedrigung entgegengewirkt, indem Wärmeenergie bei der Bildung von Distickstofftetraoxid frei wird.
Durch gezielte Temperaturänderungen lassen sich also ebenfalls chemische Gleichgewichte verschieben und sogar chemische Reaktionen erzwingen.
Bezieht man die Erkenntnisse des Massenwirkungsgesetzes in die Betrachtungen mit ein, lässt sich zusammenfassen:
Bei vielen Reaktionen lässt sich die Stoffausbeute durch Veränderung des Druckes, der Temperatur und durch die Konzentrationen von Ausgangsstoffen oder Produkten stark beeinflussen.
Beeinflussung durch die Konzentration
Durch die Änderung der Konzentrationen der Ausgangstoffe oder Reaktionsprodukte lässt sich die Ausbeute einer chemischen Reaktion ebenfalls beeinflussen. Dadurch wird jedoch nicht die Lage des Gleichgewichts geändert, denn die Gleichgewichtskonstante k bleibt unverändert. Die Ausbeute wird dadurch erhöht, sodass das Gleichgewicht gestört wird und versucht, diesem äußeren Zwang auszuweichen. Die Erhöhung der Konzentration eines Stoffes begünstigt somit die Reaktion, bei der dieser Stoff verbraucht wird. Erniedrigt man die Konzentration eines Stoffes, z. B. durch Entnahme aus dem System, so wird die Reaktion begünstigt, bei der dieser Stoff gebildet wird.
Als Beispiel soll das Löslickeitsgleichgewicht von Silberchlorid betrachtet werden:
Erhöht man die Konzentration der Chlorid-Ionen in einer gesättigten AgCl-Lösung durch Zusatz einer KCl-Lösung, so weicht das Gleichgewicht diesem Zwang aus. Unter Verbrauch der Chlorid-Ionen wird Silberchlorid ausgefällt und die – und damit die Löslichkeit des Salzes – sinkt. Der gleiche Effekt wird beobachtet, wenn man die Konzentration des anderen „Reaktionsprodukts“, der erhöht. In diesem Fall entspricht die Löslichkeit des Silberchlorids der .
Die Erhöhung der Konzentration einer Ionensorte durch gleichionige Zusätze führt zu einer Verringerung der Löslichkeit eines Salzes, weil das Löslichkeitsprodukt konstant bleibt.
Gekoppelte Gleichgewichte
Die Löslichkeit von Stoffen kann durch Zugabe von Säuren oder Komplexbildnern beeinflusst werden. In beiden Fällen liegt neben dem Löslichkeitsgleichgewicht ein weiteres chemisches Gleichgewicht vor und man spricht von gekoppelten Gleichgewichten.
Viele schwer lösliche Salze können durch Zugabe von Säuren oder Basen in Lösung gebracht werden. Die Ursache liegt darin, dass eine Ionensorte aus dem Löslichkeitsgleichgewicht gleichzeitig an einem Säure-Base-Gleichgewicht beteiligt ist.
Die schwer löslichen Sulfide sind die Salze der schwachen Säure Schwefelwasserstoff. Wenn man Eisensulfid durch Zugabe einer Säure auflösen will, liegen folgende Gleichgewichte vor.
Die Gleichgewichtskonstante der Protolyse der ergibt sich aus den beiden Säurekonstanten der zweiwertigen Säure
Durch Zugabe der Säure wird die im Säure-Base-Gleichgewicht erhöht und dadurch mehr Schwefelwasserstoff gebildet. Dazu werden dem Löslichkeitsgleichgewicht Sulfid-Ionen entzogen. Diese müssen durch Auflösen des Eisensulfids nachgebildet werden. Da Schwefelwasserstoff eine schwache Säure ist, liegt das Säure-Base-Gleichgewicht weit auf der Seite des Schwefelwasserstoffs und Eisensulfid wird bei hohen vollständig aufgelöst.
In der gleichen Weise kann die Löslichkeit eines schwer löslichen Salzes auch durch Zugabe von Komplexbildnern deutlich vergrößert werden. In diesem Fall wird ein Löslichkeitsgleichgewicht mit einem Komplexbildungsgleichgewicht gekoppelt.
Silberhalogenide sind in Ammoniak unterschiedlich löslich, da sich die Löslichkkeitsprodukte um mehrere Größenordnungen voneinander unterscheiden. Diese Tatsache macht man sich beim qualitativen Nachweis der Halogenid-Ionen zunutze.
So löst sich ein Niederschlag von Silberchlorid in Ammoniakwasser, wobei sich der lösliche Silberdiammin-Komplex bildet:
Dem Löslichkeitsgleichgewicht des Silberchlorids werden die durch die Komplexbildung entzogen. Diese werden durch Auflösen des festen Niederschlages nachgebildet, bis das der Niederschlag vollständig verschwunden oder das Löslichkeitsprodukt wieder erreicht ist. Während sich in einem Liter Wasser nur Silberchlorid lösen, sind in einem Liter einer 4 molaren Ammoniaklösung 0,16 mol des Salzes löslich.
-
Die Reaktionstemperatur beeinflusst das Konzentrationsverhältnis der im Gleichgewicht liegenden Gase: farbloses Distickstofftetraoxid und dunkelbraunes Stickstoffdioxid.