Die kinetisch-statistische Betrachtungsweise
In der Thermodynamik oder Wärmelehre ist es üblich, zur Beschreibung der Zustände oder Vorgänge in einem thermodynamischen System unterschiedliche Betrachtungsweisen anzuwenden. Neben der phänomenologischen Betrachtungsweise wird die kinetisch-statistische Betrachtungsweise genutzt. Sie ist dadurch gekennzeichnet, dass zur Beschreibung von Sachverhalten und Vorgängen Teilchengrößen genutzt werden und die Beschreibung mit statistischen (stochatischen) Gesetzen erfolgt, die sichere Voraussagen über die Gesamtheit der Teilchen eines Systems ermöglichen, nicht aber über das Verhalten des einzelnen Teilchens.
Die kinetisch-statistische Betrachtungsweise ist eine Beschreibungsweise, die gut geeignet ist, um zum Wesen thermodynamischer Erscheinungen vorzudringen. Sie ist auch die historisch jüngere Betrachtungsweise und ist diejenige, die in der kinetischen Wärmetheorie angewendet wird.
Das Wesen der kinetisch-statistischen Betrachtungsweise
Wie bereits der Name sagt, ist die kinetisch-statistische Betrachtungsweise dadurch gekennzeichnet, dass Zustände und Erscheinungen mit Teilchenmodellen beschrieben werden. Die kinetisch-statistische Betrachtungsweise lässt sich dann folgendermaßen charakterisieren:
- Es wird von der Anzahl und der Bewegung der Teilchen ausgegangen, aus denen ein Körper oder ein System aufgebaut ist.
- Die Beschreibung erfolgt mit Teilchengrößen, z.B. mit der Teilchenanzahl, der räumlichen Verteilung der Teilchen, ihrer Geschwindigkeitsverteilung und ihrer Energieverteilung.
- Zusammenhänge werden in Form statistischer Gesetze erfasst. Statistische Gesetze ermöglichen im Unterschied zu dynamischen Gesetzen zwar eindeutige Aussagen über das Verhalten oder die Eigenschaften der Gesamtheit einer großen Teilchenanzahl, nicht aber über die einzelnen Teilchen. Über einzelne Teilchen können nur Wahrscheinlichkeitsaussagen getroffen werden.
Zusammenfassend kann man formulieren:
Die Beschreibung thermodynamischer Systeme mithilfe mikroskopischer Größen (Teilchengrößen) und ihre Charakterisierung durch statistische (stochatische) Gesetze wird als kinetisch-statistische Betrachtungsweise bezeichnet.
Damit werden auch Schwankungserscheinung erfassbar, die sich einer phänomenologischen Betrachtungsweise entziehen.
-
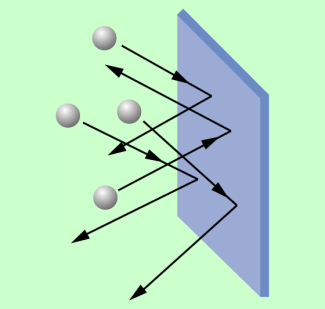
Der Druck eines Gases auf eine Fläche kann kinetisch-statistisch als eine Vielzahl von elastischen Stößen der Gasteilchen gegen die Wand gedeutet werden.
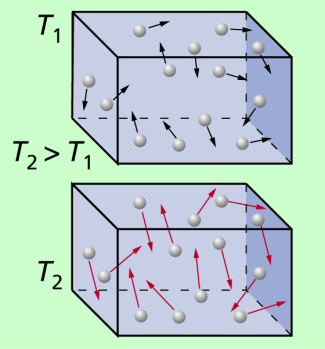
Beispiel 1: Die Temperatur soll kinetisch-statistisch gedeutet werden. Genauere Untersuchungen ergeben, dass zwischen Temperatur und Teilchenbewegung ein enger Zusammenhang besteht (Bild 2): Die Temperatur eines Körpers ist ein Maß für die mittlere kinetische Energie der Teilchen eines Körpers. Einem einzelnen Teilchen kann keine Temperatur zugeordnet werden.
Beispiel 2: Der Druck, den ein Gas auf die Wände eines Gefäßes ausübt, kann als eine Vielzahl von elastischen Stößen der Gasteilchen gegen die Gefäßwand gedeutet werden (Bild 1). Wie stark dabei ein einzelnes Teilchen gegen die Gefäßwand stößt, ist relativ uninteressant.
Anwendungsbereich der kinetisch-statistischen Betrachtungsweise
Grundsätzlich gilt, dass man eine bestimmte Erscheinung sowohl kinetisch-statistisch als auch phänomenologisch beschreiben kann. So kann man z.B. den thermischen Zustand phänomenologisch durch die Temperatur, kinetisch-statistisch durch die mittlere kinetische Energie aller Teilchen kennzeichnen. Der Druck in einem Gas lässt sich als Zahlenwert angeben oder als Stöße von Teilchen interpretieren.
In den meisten Fällen ist es eine Frage der Zweckmäßigkeit und der Zielstellung, welche Beschreibungsweise man nutzt.
Die kinetisch-statistische Beschreibungsweise wird vor allem dann angewendet, wenn man - so wie das in der kinetischen Gastheorie geschieht - zum Wesen von Erscheinungen vordringen will. Dabei ist es aber notwendig, mit Modellen zu arbeiten, z.B. bei Gasen mit dem Modell ideales Gas.
Grundsätzlich gilt: Phänomenologische und kinetisch-statistische Betrachtungsweise ergänzen einander. Sie können auf ein- und dieselben Prozesse und Erscheinungen angewendet werden. Welche der Betrachtungsweise man jeweils nutzt, hängt von den gegebenen Bedingungen und Zielen ab.
-
Die Temperatur kann als Maß für die mittlere kinetische Energie der Teilchen und damit für ihre mittlere Geschwindigkeit gedeutet werden.