Zusammensetzung des Bodens
Der Boden ist ein komplexes Gemisch aus anorganischen Bestandteilen, abgestorbenem organischen Material (Humus), Bodenluft und Bodenwasser mit gelösten anorganischen und organischen Substanzen.
Die anorganischen Anteile sind hauptsächlich Silicate, große Bedeutung haben Tonmineralien als Speicher für Pflanzennährstoffe. Abgestorbenes organisches Material wird von Bodenorganismen in Huminstoffe umgewandelt, die dann weiter abgebaut werden. Sie sind die wichtigste natürliche Quelle für Stickstoffdünger, außerdem besitzen sie viele funktionelle Gruppen, die Kationen binden können.
Die Lithosphäre (griechisch lithos = Stein) ist die Gesteinshülle der oberen festen Erdkruste. Der Boden, die relativ lockere Schicht wird auch als Pedosphäre (griechisch pedon = Boden) bezeichnet.
Während die Atmosphäre und die Hydrosphäre eine verhältnismäßig einheitliche stoffliche Zusammensetzung aufweisen, ist das beim Boden völlig anders. Er ist keine einheitliche Materie, sondern ein kompliziert zusammengesetztes System aus mineralischen und organischen Bestandteilen mit Pflanzenwurzeln, Bodenorganismen und Hohlräumen, in denen sich Luft und Wasser befinden.
Die mineralischen Bestandteile werden einerseits durch die Verwitterung von Gesteinen gebildet, zum anderen entstehen sie beim Abbau abgestorbener Biomasse durch Bodenorganismen zu anorganischen Verbindungen. Dieser Vorgang wird als Mineralisation bezeichnet.
Die organischen Bodenbestandteile, der Humus, entstehen durch chemische Reaktionen oder durch Mikroorganismen aus abgestorbener Biomasse, die Humifizierung.
| abgestorbene Biomasse | |||
| Umwandlung | geologisch | chemisch und biologisch | biologisch |
| Vorgang | Inkohlung | Humifizierung | Mineralisierung |
| Entstehung von | fossilen Brennstoffen | Huminstoffen | Mineralstoffen |
Zusammensetzung
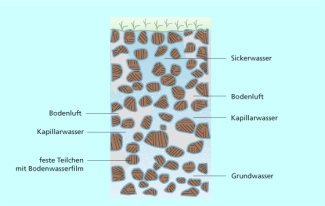
Die Böden in Mitteleuropa bestehen zu etwa 50 % aus festen Bestandteilen und 50 % aus Poren. Diese sind jeweils etwa zur Hälfte mit Bodenwasser und Bodenluft gefüllt. Im Bodenwasser sind Nährstoffe und organische Substanzen gelöst.
Bei den festen Bestandteilen nehmen 40-47 % die mineralischen Anteile ein, 3-10 % sind organische Substanzen. Torfböden können mehr als 25 % organische Substanz enthalten (Bild 2).
Mineralische Bestandteile
Die mineralischen Bestandteile des Bodens sind hauptsächlich Silicate. Unter diesen sind die Tonmineralien besonders wichtig. Weiterhin gehören zum mineralischen Teil des Bodens die anorganischen Pflanzennährstoffe, vor allem die Kationen Ca2+, Mg2+ und K+, sowie Nitrat und Phosphat. Die Kationen sind teilweise an die Tonmineralien gebunden.
Die Tonmineralien sind schichtförmig aufgebaute quellfähige Aluminiumsilikate, die Wassermoleküle in ihrer Struktur enthalten und die Nährstoff-Kationen binden können.
Die wichtigsten Tonmineralien sind der Kaolinit und der Montmorillonit
Kommt es im Gitter des Montmorillonits zum Austausch von Aluminium-Ionen durch Magnesium-Ionen, werden andere Nährstoff-Kationen zum Ladungsausgleich zwischen die Schichten eingelagert.
Zwischen die Schichten der Tonmineralien können aber nicht nur Nährstoff-Kationen sondern auch organische Verbindungen wie Biozide wie Insektizide, Pestizide oder Herbizide eingelagert werden.
Organische Substanzen
Die im Boden enthaltene abgestorbene pflanzliche und tierische Biomasse wird als Humus bezeichnet. Humus besteht aus hochmolekularen Huminstoffen verschiedener Zusammensetzung, die durch chemische und biochemische Prozesse ständig auf-, ab- und umgebaut werden. Letztendlich werden sie durch Mikroorganismen mittels Luftsauerstoff zu Kohlenstoffdioxid, Wasser und Nitrat abgebaut, d. h. mineralisiert.
Huminstoffe besitzen eine große Oberfläche und haben in ihrer Struktur viele polare funktionelle Gruppen. Dadurch sind sie in der Lage, Wasser und Kationen, als Nährstoffe zu binden. Es können andererseits aber auch Schwermetalle gebunden werden.
| Wichtige funktionelle Gruppen der Huminstoffe | |
| Carboxy-Gruppe | -COOH |
| Carbonyl-Gruppe | -CO- |
| Hydroxy-Gruppe | -OH |
| Amino-Gruppe | |
| Imino-Gruppe | -NH- |
Huminstoffe sind gelb bis schwarz gefärbt und teilweise wasserlöslich. Die dunkle Farbe des Wassers z. B. in Moorgebieten wird von gelösten Huminstoffen verursacht.
Huminstoffe sind die wichtigste natürliche Quelle für die Stickstoffversorgung der Pflanzen. Ferner regulieren sie den Kationenaustausch des Wasser- und Nährstoffhaushaltes des Bodens.
Huminstoffe und Tonmineralien sind über chemische Bindungen zum sogenannten „Ton-Humus-Komplex“ miteinander verbunden, wobei die Huminstoffe für die Bindung von Nährstoffen eine größere Wirksamkeit haben als die Tonmineralien. Die wichtigsten Pflanzennährstoffe sind die Kationen sowie Nitrat und Phosphat.
In Mitteleuropa enthalten Ackerböden meist 1-2 % Huminstoffe, die sogenannten Schwarzerdeböden bis zu 7 % und Weideboden bis 10 % Humus.
Da Humus letztlich mineralisiert wird, und Pflanzen während des Wachstums Nährstoffe verbrauchen, muss man landwirtschaftlich genutzten Böden diese Stoffe immer wieder durch Düngung zuführen.
-
Der Boden besteht zu etwa 50 % aus festen Bestandteilen und 50 % aus Poren, die das Bodenwasser und die Bodenluft enthalten.
Bodenbelastung
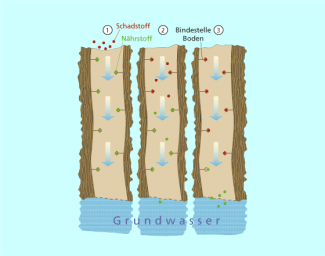
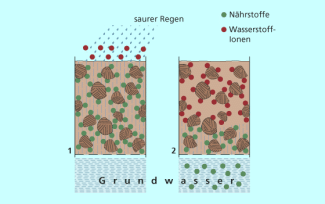
Belastungen des Bodens erfolgen hauptsächlich durch den sauren Regen (Bild 3), Schwermetalle, Düngemittel und Biozide. Diese Schadstoffeinträge in den Boden können in mehrfacher Weise wirken.
Mögliche negative Wirkungen von Bodenbelastungen können sein:
- schädliche Wirkungen für Pflanzen und Bodenorganismen
- Auswirkungen für Tier und Mensch über die Nahrungskette
- Auswaschen der Schadstoffe ins Grundwasser und damit Gefährdung des Trinkwassers (Bild 4)
Daher ist es sehr wichtig, in der Landwirtschaft Düngemittel und Pflanzenschutzmittel sinnvoll, d. h. optimal und nicht maximal einzusetzen.
-
Saurer Regen hat Auswirkung auf die Boden- und Grundwasserqualität.
-
Schadstoffeintrag in den Boden