Legierungen
Legierungen sind Stoffgemische von meist zwei oder mehreren Metallen, die andere Eigenschaften als die sie bildenden reinen Metalle aufweisen.Durch Zusammenschmelzen verschiedener Metalle oder durch Diffusion eines zweiten Metalles in das Grundmetall bei höherer Temperatur erfolgt die Bildung von Legierungen.
Mitunter werden auch geringe Mengen Nichtmetalle wie Kohlenstoff, Bor, Silicium (Bildung von Einlagerungen auf Zwischengitterplätzen) zugesetzt. Legierungen sind z. B. Stahl, Bronze, Messing, Neusilber, Duraluminium.
Viele Metalle besitzen für die technischen Anwendungen nicht die notwendige Härte, Bruchfestigkeit, Korrosionsbeständigkeit oder Dichte. Mit der Herstellung von Legierungen kann dieses Problem gezielt gelöst werden.
Herstellen und Eigenschaften von Legierungen
Beim Zusammenschmelzen von Metallen (Legierungsmetalle) bilden sich häufig Mischungen, die auch nach dem Erstarren als solche erhalten bleiben. Es haben sich Legierungen (lat. ligare = verbinden) gebildet. Auch durch Diffusion eines zweiten Metalle in das Gitter des Grundmetalls bei höheren Temperaturen können sich Legierungen bilden, wobei besonders die Oberflächeneigenschaften, z. B. Härte, des Grundmetalls erhöht werden kann. Auch die Einlagerung von Nichtmetallatomen (Kohlenstoff, Silicium z. B. im Stahl) in das Gitter des Grundmetalls wird zur gezielten Veränderung der Eigenschaften genutzt.
Beim Mischen von Metallen können sich homogene Legierungen (unbegrenzte Mischbarkeit) z. B. Kupfer-Gold oder Kupfer-Silber bilden, die aus einer Phase mit einem einheitlichen Kristallgitter bestehen. Solche Legierungen bilden Metalle mit gleichem Gittertyp (kubisch dichte Packung), ähnlichem Atomradius und vergleichbarer Elektronegativität.
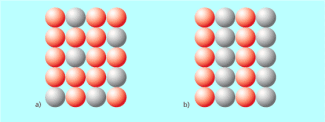
Dabei können die Atome des zweiten Metalls statistisch im Gitter des Grundmetalls verteilt sein (Bild 3a). Das geschieht oft dann, wenn sich die Größe der Atome beider Metalle nur wenig unterscheidet. Ein Beispiel dafür ist Messing. Die Zinkatome mit einem Durchmesser von 266 pm sind nicht viel größer als die Kupferatome mit 255 pm Durchmesser. Daher kann Kupfer bis zu 38 % Zinkatome im Gitter aufnehmen.
Neben der statistischen Verteilung gibt es auch Legierungen mit geordneter Verteilung der verschiedenen Metalle. So bilden sich bei Kupfer-Gold-Legierungen sogenannte Überstrukturen mit abwechselnden Schichten der beiden Metalle im Gitter (Bild 3b)
Heterogene Legierungen bestehen dagegen aus einem Metallgefüge, das aus mehreren metallischen Phasen besteht, z. B das Gemisch aus Zinn und Blei, das wegen seines niedrigen Schmelzpunkts als Lot verwendet wird (Lötzinn).
Die strukturelle Vielfalt der Metallgitter, die Variabilität der Valenzelektronen der die Legierungen bildenden Metalle und die unterschiedliche Elektronegativität der Metalle führt zu einer sehr großen Zahl von Legierungen bei denen auch solche mit diskreter stöchiometrischer Zusammensetzung wie CaMg oder MgSn auftreten.
Verschiedene Legierungen
Messing ist eine Legierung aus über 55 % Kupfer und Zink. Je nach Anteilen der Bestandteile unterscheidet man verschiedene Messingarten, z. B. Gelbguss, Weißguss oder Tombak.
Die Legierung Bronze enthält mindestens 60% Kupfer und als zweiten Hauptbestandteil Zinn.
Während die Reinstoffe Kupfer, Zink und Zinn relativ weich sind, erreichen die Legierungen Bronze und Messing eine wesentlich größere Härte. Das wurde bereits in der vorgeschichtlichen Bronzezeit erkannt, obwohl es vielleicht dem zufälligen gemeinsamen Schmelzen von Kupfer- und Zinnerzen zu verdanken ist, dass die Bronze so frühzeitig in der geschichtlichen Entwicklung der Menschheit gefunden wurde (4 000 v. Chr.).
Messing besitzt eine gute Korrosionsbeständigkeit und kann wegen seiner größeren Härte durch Drehen und Fräsen besser mechanisch bearbeitet werden als Kupfer.
Die größere Härte der Legierungen lässt sich damit erklären, dass die einzelnen Atomschichten im Gitter bei Anwesenheit von Atomen unterschiedlicher Größe sich nicht mehr so leicht gegeneinander verschieben lassen.
Für die Industrie, das Bauwesen und andere Wirtschaftszweige sowie für den Gebrauch im Alltag sind die festeren, beständigen und elastischen Eisenlegierungen bedeutsam.
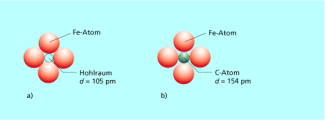
Stahl ist eine Legierung aus Eisen mit verschiedenen Zusätzen. Wesentlich ist, dass Stahl einen Kohlenstoffanteil von maximal 1,6 % enthält. Dadurch wird er hart, elastisch und schlagfest. Er lässt sich gießen, schmieden, pressen, walzen. Da die Kohlenstoffatome deutlich kleiner als die Eisenatome sind, werden sie in Hohlräume zwischen den dicht gepackten Eisenatomen im Gitter eingelagert (Bild 4a und 4b). Dadurch wird das Eisengitter etwas aufgeweitet. Der Kohlenstoffgehalt verleiht dem Stahl Härte und Festigkeit bei gleichzeitiger Verformbarkeit. Steigt der Kohlenstoffgehalt aber über 2 %, wird das Eisen spröde und ist nicht mehr schmiedbar. Auch andere kleine Atome (Bor, Stickstoff, Phosphor) können in gleicher Weise in Metallgitter eingelagert werden und erhöhen die Härte des Metalls.
Durch Zusatz von Mangan, Nickel, Chrom, Wolfram und anderen Stoffen können die Eigenschaften von Stahl beeinflusst werden.
Unlegierte Stähle sind meist einfache Kohlenstoffstähle (Massenstähle). Niedrig legiert sind Stähle mit einem Legierungsanteil von bis zu 5 %, hoch legiert sind Stähle mit einem Legierungsanteil von über 5 % (Edelstähle, V2A-Stahl: Chrom, Nickel, Eisen).
Die bei Raumtemperatur flüssigen oder festen Quecksilberlegierungen werden als Amalgame (arabisch: al malgam = erweichende Salbe) bezeichnet. Gold und Silber lösen sich in Quecksilber, so dass diese Amalgambildung verbreitet zur Anreicherung der Edelmetalle genutzt wurde. Zinn-Kupfer-Edelmetall-Amalgame zeichnen sich durch Härte und Bruchfestigkeit aus (Zahntechnik).
Weitere Legierungen von Metallen, die wirtschaftliche Bedeutung besitzen, sind u. a.
- Neusilber: Zink, Kupfer, Nickel
- Duraluminium: Aluminium, Kupfer, Magnesium, Mangan
![]()
-
Grundprinzipien der Legierungsbildung
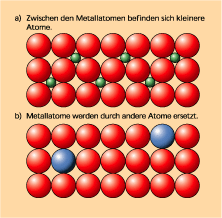
-
Legierungen: statistische (a) und geordnete (b) Verteilung der Atome im Metallgitter
-
Die eingelagerten Kohlenstoffatome verleihen dem Stahl Härte und Festigkeit bei gleichzeitiger Verformbarkeit.