Modelle
Ein Modell in der Chemie ist ein ideelles (gedankliches) oder materielles (gegenständliches) Objekt, das als Ersatzobjekt für ein Original genutzt wird. Es ist eine Vereinfachung des Originals und damit der Wirklichkeit. In einigen Eigenschaften stimmt das Modell mit dem Original überein, in anderen nicht. Ein Modell ist weder richtig noch falsch, sondern nur für einen bestimmten Zweck geeignet oder nicht geeignet.
Beispiele für Modelle sind Atommodelle, das Teilchenmodell, Kalottenmodelle von der Struktur von Stoffen oder Modelle von technischen Geräten und Anlagen.
-
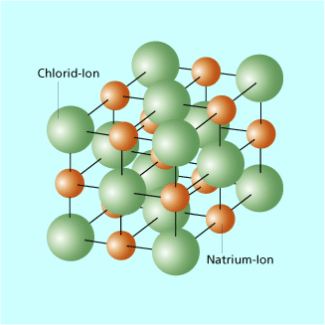
Gittermodell des Natriumchloridkristalls
Funktionen von Modellen
Modelle können unterschiedliche Funktionen erfüllen.
Modelle sind ein Mittel zur Gewinnung neuer Erkenntnisse. Man kann mithilfe eines Modells Erscheinungen erklären und voraussagen. So kann man z. B. mit dem Teilchenmodell erklären, wie es zur Durchmischung zweier Flüssigkeiten kommt.
-
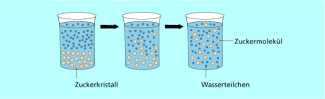
Lösen von Zucker in Wasser
- Modelle sind ein wichtiges Mittel zur Veranschaulichung von Sachverhalten. So kann man sich z. B. mithilfe eines Kalottenmodells die Struktur der Teilchen eines Stoffs veranschaulichen und besser vorstellen.
- Modelle technischer Geräte und Anlagen ermöglichen es, den grundsätzlichen Aufbau und die Wirkungsweise eines Gerätes vereinfacht und überschaubar darzustellen.
- Modelle sind ein Mittel zur Überprüfung der Funktion einer technischen Konstruktion. So kann man z. B. chemisch-technische Anlagen zur industriellen Gewinnung von Stoffen zunächst mit Laboraufbauten in ihrer Funktion überprüfen.
-
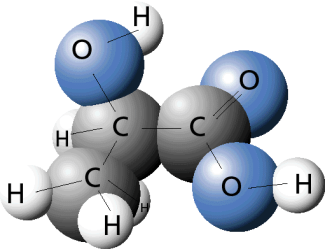
Kalottenmodell
Arten von Modellen
Modelle können sowohl materiell (gegenständlich) als auch ideell (gedanklich) sein. Beispiele für materielle Modelle sind das Modell eines Verbrennungsmotors oder ein aus Kugeln aufgebautes Teilchenmodell (Kalottenmodell, siehe Bild 3).
Beispiele für ideelle Modelle sind das Teilchenmodell als System von Aussagen und Atommodelle.
Es ist auch möglich, für ein bestimmtes Original verschiedene Modelle zu schaffen, die das Original mehr oder weniger gut widerspiegeln. Ein Beispiel dafür sind verschiedene Atommodelle. Bei technischen Modellen wird man das Modell weitgehend in Abhängigkeit vom jeweiligen Verwendungszweck gestalten.
-
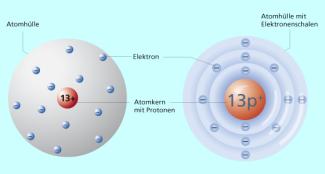
verschiedene Atommodelle des Al-Atoms
Modellexperimente
Mit materiellen Modellen kann man auch experimentieren. Man bezeichnet solche Experimente als Modellexperimente. Darüber hinaus kann man mit ihnen Erscheinungen erklären und voraussagen.
Beispiel: Mischt man 50 ml Alkohol (Ethanol) und 50 ml Wasser, so hat das Gemisch aus beiden nicht ein Volumen von 100 ml, sondern nur von 96 ml (Bild 6). Das kann man in einem Modellexperiment bestätigen und damit zugleich eine anschauliche Erklärung für diese Erscheinung finden.
Bei einem Modellexperiment nimmt man als Ethanolmoleküle Erbsen (größere Teilchen, also größere Kugeln) und anstelle der Wassermoleküle Reiskörner (kleinere Teilchen, also kleinere Kugeln), dann kann man ein bestimmtes Volumen Erbsen und ein bestimmtes Volumen Reis mischen. Das Volumen des Gemischs ist deutlich kleiner als die Summe der beiden Einzelvolumina. Die Ursache dafür liegt darin, dass die Reiskörner die Lücken zwischen den Erbsen ausfüllen und damit die Teilchen insgesamt einen kleineren Raum einnehmen.
Dieser Vorgang vollzieht sich auch bei der Mischung von Ethanol und Wasser. Er geht dort aber mit den nicht sichtbaren Molekülen vonstatten.
Das Mischungsvolumen hängt nicht allein von der unterschiedlichen Größe der Teilchen, sondern auch von der Stärke der Wechselwirkungen verschiedener Teilchen ab. Es gibt auch Gemische, bei denen das Mischungsvolumen größer ist.
-
Mischung von Ethanol und Wasser

Heinz Mahler, Berlin

