Molekül
Moleküle sind nach außen elektrisch neutrale Teilchen, die aus mindestens zwei Atomen aufgebaut sind.
Die Atome sind untereinander durch Elektronenpaarbindung (Atombindung) verknüpft.
Je nach Anzahl der Atome unterscheidet man zwischen zweiatomigen Molekülen, mehratomigen (n > 2 Atome) und Makromolekülen, die oft aus mehr als 1000 Atomen aufgebaut sind.
Elektrisch neutrale Teilchen, die aus mindestens zwei Atomen bestehen, werden Moleküle genannt.
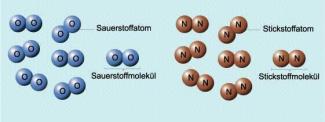
Ein Molekül Sauerstoff besteht aus zwei miteinander verbundenen Sauerstoffatomen, die durch unpolare Atombindungen miteinander verknüpft sind.
Ein Molekül Stickstoff besteht aus zwei miteinander verbundenen Stickstoffatomen. Auch hier werden die Atome durch bindende Elektronenpaare zusammen gehalten.
Bei den Stoffen Sauerstoff und Stickstoff handelt es sich nicht um chemische Verbindungen, denn die Moleküle sind nur aus einer Atomsorte zusammengesetzt.
-
Die Elemente Sauerstoff und Stickstoff treten hauptsächlich in Form zweiatomiger Moleküle auf.
Auch neutrale Teilchen, die aus mehreren Atomarten bestehen, nennt man Moleküle. Im Gegensatz zu den oben genannten Beispielen handelt es sich jedoch dabei um Molekülverbindungen.
Ein typisches Beispiel für eine solche chemische Verbindung ist Wasser. Die Verbindung kann durch eine chemische Reaktion in die Elemente Sauerstoff und Wasserstoff zerlegt werden.
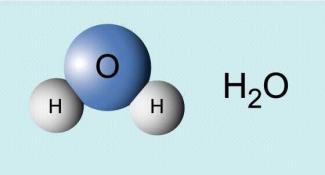
Aus der Formel und aus dem räumlichen Modell des Wassermoleküls erkennt man, dass pro Molekül je ein Sauerstoffatom mit je zwei Wasserstoffatomen verbunden ist.
Eine Formel gibt an, aus welchen Elementen der Stoff aufgebaut ist und in welchem Verhältnis die Atome miteinander verbunden sind.
-
einfaches räumliches Modell und Formel des Wassermoleküls
Die Größe und die Eigenschaften von Molekülen können stark variieren. Man unterscheidet zweiatomige Moleküle , Moleküle mit mehr als zwei Atomen und Makromoleküle (Cellulose, Eiweiße, PVC) , die mehrere Tausend Atome enthalten können.
Zweiatomige Moleküle aus gleichen Atomen sind in der Regel Gasmoleküle. Manche Elementsubstanzen wie Schwefel oder Phosphor bilden aber mehratomige, unpolare Moleküle aus, die unter Normalbedingungen zu Feststoffen kristallisieren.
Bestehen die Moleküle aus verschiedenen Atomsorten, dann liegt eine mehr oder weniger polare Atombindung vor. Je höher die Polarität und die molare Masse einer Molekülverbindung ist, um so höher ist in der Regel ihr Schmelzpunkt und ihr Siedepunkt.
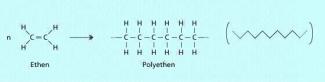
Deshalb nimmt beispielsweise der Siedepunkt der Alkane mit der Anzahl der Kohlenstoffatome im Molekül zu. Makromoleküle wie Cellulose oder der Kunststoff Polyethylen (PE) bestehen aus mehreren Tausend Atomen und sind unter anderem aufgrund ihres hohen Molekülgewichts Feststoffe.
-
Die Art und die Anzahl der Atome im Molekül bestimmen dessen Eigenschaften.

-
Polyethylen kann aus 1 000 bis 10 000 Ethenmolekülen bestehen.