Trennungsgänge
Ein Trennungsgang wird durchgeführt, wenn man ermitteln möchte, welche Bestandteile ein Stoffgemisch enthält, oder wenn man mit möglichst reinen Stoffen arbeiten will.
Der Trennungsgang ist Teil einer chemischen Analyse und erleichtert den Nachweis einzelner Stoffe.
Trennverfahren wurden entwickelt, um Stoffgemische in ihre Einzelbestandteile zerlegen zu können, damit man diese dann untersuchen beziehungsweise weiter verarbeiten kann.
Man nutzt dabei hauptsächlich die unterschiedlichen physikalischen Eigenschaften der einzelnen Bestandteile.
Beispiele für Trennprozesse sind Sieben, Dekantieren (Trennen durch Abgießen), Zentrifugieren, Filtrieren, Abdampfen, Destillation, Kristallisation (Ausfällen von Kristallen aus einer Lösung), Chromatografie, Extraktion (Herauslösen eines Stoffes durch ein geeignetes Lösungsmittel), sowie viele weitere Verfahren.
Trennungsgänge
Trennungsgänge sind chemische Verfahren zur Auftrennung von Stoffgemischen und dienen in der Regel zur Vereinfachung der chemischen Analyse von Stoffgemischen. Nach der Trennung können die einzelnen Bestandteile des Gemischs einfacher nachgewiesen werden, da sich verschiedene Ionen bei den Nachweisreaktionen stören.
Trennt man die störenden Ionen ab, so können diese die Nachweisreaktionen anderer Ionen nicht mehr behindern.
Die einzelnen Gruppen enthalten Ionen, die mit geeigneten Reagenzien (Stoffe die bestimmte Reaktionen erzeugen) ähnlich reagieren und sich deswegen gemeinsam abtrennen lassen.
Anschließend trennt man die einzelnen Gruppen weiter auf, um das Vorhandensein der Ionen bestimmter Elemente zu überprüfen.
Man unterscheidet Kationen- und Anionentrennungsgänge, aber auch in der organischen Chemie werden Trennungsgänge zur Isolierung von Molekülverbindungen genutzt.
Vorproben als Hilfsmittel
Man kann mithilfe von charakteristischen Vorproben schon vor Beginn eines Trennungsgangs Hinweise auf die Bestandteile eines Stoffgemisches bekommen.
Es kann auch sein, dass man durch die Ergebnisse der Vorproben den Trennungsgang vereinfachen kann.
Das ist beispielsweise dann möglich, wenn die Vorprobe auf eine bestimmte Ionengruppe negativ war. Dann braucht man diese Gruppe im Trennungsgang auch nicht abzutrennen.
Vorproben sind zum Beispiel die Flammenfärbung oder die Spektroskopie.
Durchführung eines Trennungsgangs
Zuerst werden die entsprechenden Vorproben durchgeführt, damit man einen Überblick über die eventuell enthaltenen Substanzen bekommt.
Die feste Analysensubstanz wird dann in einem geeigneten Lösungsmittel gelöst.
Bleiben trotzdem unlösliche Bestanteile übrig, so werden diese abgetrennt und speziell untersucht.
Im darauf folgenden Trennungsgang werden nun die einzelnen Ionengruppen der jeweiligen Elemente mit den entsprechenden Reagenzien von der Lösung abgetrennt. Die Gruppen werden dabei als Niederschläge aus der Lösung durch Fällungsreaktionen isoliert, es bilden sich feste Verbindungen.
Diese Niederschläge filtriert man ab und untersucht sie getrennt von der Lösung.
Die Verbindungen werden weiter zerlegt und die einzelnen Bestandteile durch charakteristische Fällungs- oder Farbreaktionen ermittelt.
-
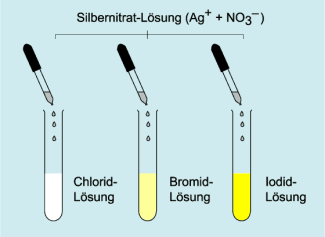
Durch Zugabe von Silbernitrat-Lösung zu einer halogenidhaltigen Lösung können Halogenid-Ionen ausgefällt werden.