Komplementarität und Komplementaritätsprinzip
Das von NIELS BOHR (1885-1962) in die Quantenphysik eingeführte Komplementaritätsprinzip kennzeichnete er selbst mit dem Satz: „Die Begriffe Teilchen und Welle ergänzen sich, indem sie sich widersprechen; sie sind komplementäre Bilder des Geschehens.“
Nach dem Komplementaritätsprinzip kann ein Interferenzmuster nur beobachtet werden, wenn die zu einem Versuchsergebnis beitragenden klassisch denkbaren Möglichkeiten nicht durch eine Messung unterscheidbar sind („Welcher-Weg“-Information). Unterscheidbarkeit erhält man z.B. dadurch, dass man Atome verwendet, die Photonen emittieren. Man hat dies in den neunziger Jahren des 20. Jahrhunderts in verschiedenen Varianten durchgeführt: Bei einem der Experimente wurden Atome an einer stehenden Lichtwelle wie an einem Gitter gebeugt. In einer anderen wurde mithilfe von zwei stehenden Lichtwellen ein Atom-Interferometer realisiert.
Was bedeutet Komplementarität?
Der dänische Physiker NIELS BOHR (1885-1962) leistete nicht nur wesentliche Arbeiten zur Entwicklung der Atomphysik, etwa mit dem bohrschen Atommodell (1913) und einer Theorie der Kernspaltung (1939), sondern auch entscheidende Beiträge zur Entwicklung und Interpretation der Quantenphysik. So formulierte er u.a. zwei grundlegende Prinzipien, das Korrespondenzprinzip und das Komplementaritätsprinzip.
Das 1918 veröffentlichte Korrespondenzprinzip besagt, dass die Quantentheorie mit der klassischen Theorie in Übereinstimmung gebracht werden kann, mit ihr „korrespondiert“. Die Quantenmechanik muss für den Grenzfall großer Massen oder großer Bahnabmessungen in die klassische Mechanik übergehen.
Das Komplementaritätsprinzip ermöglicht eine widerspruchsfreie Deutung quantenmechanischer Erscheinungen. BOHR selbst formulierte:
„Die Begriffe Teilchen und Welle ergänzen sich, indem sie sich widersprechen; sie sind komplementäre Bilder des Geschehens.“
Erstmals vorgestellt hat BOHR dieses Prinzip auf einer Physiker-Versammlung, die 1927 zu Ehren des 100. Todestages von ALESSANDRO VOLTA (1745-1827) in dessen Geburts- und Sterbeort Como stattfand. Eine erste Veröffentlichung dazu erschien in der Zeitschrift „Nature“ in englischer Sprache. In deutscher Fassung wurden die grundlegenden Ausführungen von BOHR 1928 in den „Naturwissenschaften“ unter dem Titel „Das Quantenpostulat und die neuere Entwicklung der Atomistik“ veröffentlicht. Diese Schrift von BOHR begründet die sogenannte Kopenhagener Deutung der Quantenphysik.
Komplementarität bei Doppelspaltexperimenten
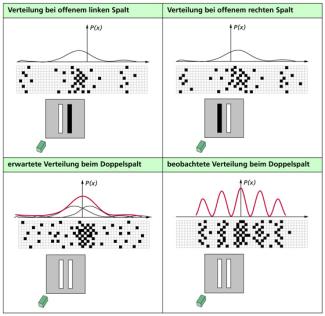
Die Unbestimmtheit von Quantenobjekten kann man als zentralen Wesenszug der Quantenphysik ansehen. Führt man z.B. mit Elektronen Doppelspalt-Experimente durch, dann ergeben sich am Einzelspalt Verteilungen, wie sie auch in der Optik bei Licht registriert werden (Bild 2 oben). Wenn man beide Spalte öffnet, erwartet man, dass das Quantenobjekt entweder durch den einen oder den anderen Spalt geht und sich damit eine Verteilung ergibt, die der Summe der beiden Einzelspaltmuster entspricht (Bild 2 unten links). Stattdessen erhält man ein Interferenzmuster, wie es aus der Optik vom Doppelspalt her bekannt ist (Bild 2 unten rechts). Diese Ergebnisse lassen sich so zusammenfassen:
Die Vorstellung, dass die Quantenobjekte beim Doppelspaltversuch durch den einen oder den anderen Spalt gehen, ist falsch. Durch welchen Spalt das Quantenobjekt beim Doppelspaltversuch geht, ist objektiv unbestimmt.
Auch an anderen Beispielen zeigt sich, dass jede anschauliche Vorstellung darüber, wie ein Quantenobjekt von einer Quelle zu einem Detektor kommt, zu Widersprüchen führt. Das ist kein Widerspruch zu der Erkenntnis, dass Messungen an unbestimmten Zuständen zu eindeutigen Messergebnissen führen.
Das Komplementaritätsprinzip
Die bohrsche Formulierung war bereits oben genannt: „Die Begriffe Teilchen und Welle ergänzen sich, indem sie sich widersprechen; sie sind komplementäre Bilder des Geschehens.“
Man kann es, wenn man von den oben beschriebenen Versuchen mit Spalten ausgeht, auch folgendermaßen formulieren:
Die Beobachtung eines Interferenzmusters und „Welcher-Spalt-Information“ schließen sich aus.
-
Registrierte und erwartete Ergebnisse beim Durchgang von Quantenobjekten durch Spalte
Neuere Experimente zur Unterscheidbarkeit
In den neunziger Jahren des 20. Jahrhunderts konnten aufgrund der fortgeschrittenen Experimentiertechnik mehrere neuartige Experimente durchgeführt werden, die bis dahin nur als Gedankenexperimente existierten. Einige dieser Experimente werden nachfolgend beschrieben.
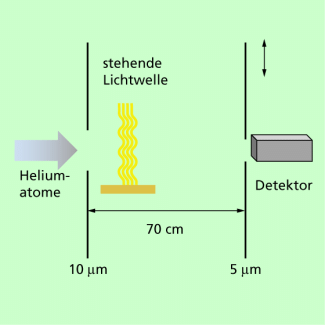
Beugung von Atomen an einer stehenden Lichtwelle nach PFAU et al.
Die stehende Lichtwelle wirkt auf die Atome wie ein Gitter. Die Frequenz der Lichtwelle kann verändert werden. Wenn die Frequenz der Lichtwelle mit einer Anregungsfrequenz der Atome übereinstimmt, kann ein Photon angeregt und wieder ausgestrahlt werden.
-
Beugung von Atomen an einer stehenden Lichtwelle
Messergebnisse für die Beugung von Atomen an einer stehenden Lichtwelle
Wenn die Lichtfrequenz nicht gerade einer Anregungsfrequenz der Atome entspricht, wird auch kein Photon wieder ausgestrahlt. Man hat keine „Welcher-Weg“-Information, das Interferenzmuster ist gut zu beobachten (gepunktete Linie).
Wird aber die Lichtfrequenz auf eine Anregungsfrequenz der Atome abgestimmt, so kann das Photon wieder ausgestrahlt werden. Je nachdem, wohin dies geschieht, kann man auf die Realisierung einer der Möglichkeiten schließen. Um dies festzustellen, könnte man z.B. Detektoren aufstellen, die die emittierten Photonen lokalisieren. Es ist aber gar nicht nötig, die „Welcher-Weg“-Information tatsächlich zu ermitteln. Es genügt, wenn sie aus den Photonen erhalten werden kann.
Das Interferenzmuster mit Photonenanregung (durchgezogene Linie) ist nicht ganz verschwunden. Dies liegt daran, dass sich nur etwa die Hälfte der Atome nach dem Lichtgitter im angeregten Zustand befindet. Die andere Hälfte ist im Grundzustand und kann deshalb auch kein Photon emittieren, das eine „Welcher-Weg“-Information trägt.
Atom-Interferometer mit zwei stehenden Lichtwellen nach DÜRR et al. (schematisch)
Wenn Atome schräg auf eine stehende Lichtwelle auftreffen, wirkt die Lichtwelle wie ein Strahlteiler für Photonen. Somit gibt es für ein Atom, das im linken Strahl ankommt zwei klassisch denkbare Möglichkeiten anzukommen, A-B-D und A-C-E. (Ebenso gibt es für den rechten Strahl die Möglichkeiten A-C-G und A-B-F.) Wenn die Möglichkeiten nicht unterscheidbar sind, erwartet man ein Interferenzmuster, ansonsten keines.
Messergebnis ohne „Welcher-Weg“-Information für das Atom-Interferometer mit zwei stehenden Lichtwellen
Ohne weitere Maßnahmen zur Unterscheidung der beiden Möglichkeiten erhält man ein Interferenzmuster (hier bestehend aus nur zwei Maxima innerhalb der Atomstrahlbreite).
Messergebnisse mit „Welcher-Weg“-Information das Atom-Interferometer mit zwei stehenden Lichtwellen
Wenn man die Möglichkeiten durch Anregung der Atome mit Mikrowellenphotonen unterscheidbar macht, beobachtet man kein Interferenzmuster mehr.

