Spezifische Wärmekapazität
Die spezifische Wärmekapazität eines Stoffes gibt an, wie viel Wärme von einem Kilogramm (1 kg) dieses Stoffes abgegeben oder aufgenommen wird, wenn sich seine Temperatur um ein Kelvin (1 K) ändert.
| Formelzeichen: | c |
| Einheit: | ein Kilojoule je Kilogramm und Kelvin |
Für Natur und Technik von besonderer Bedeutung ist die spezifische Wärmekapazität von Wasser.
Magma quillt aus dem Erdinneren und kühlt sich allmählich ab. Dabei gibt es Wärme an die Umgebung ab. Seine thermische Energie verringert sich.
Wenn wir heißes Wasser brauchen, so müssen wir dem aus der Leitung entnommenen Wasser Wärme zuführen, indem wir es z. B. auf eine Herdplatte stellen. Das Wasser nimmt Wärme auf. Seine thermische Energie vergrößert sich.
Die Wärme, die von einem Körper an seine kältere Umgebung abgegeben oder die von einem Körper aufgenommen wird, ist abhängig von
- dem Stoff, aus dem der Körper besteht,
- der Masse des Körpers und
- der Temperaturdifferenz zwischen der Endtemperatur und der Anfangstemperatur des Körpers.
Die Zusammenhänge zwischen den verschiedenen Größen sind in der Grundgleichung der Wärmelehre beschrieben. Die Abhängigkeit der abgegebenen oder aufgenommenen Wärme vom jeweiligen Stoff wird durch die spezifische Wärmekapazität charakterisiert. Allgemein gilt:
Die spezifische Wärmekapazität eines Stoffes gibt an, wie viel Wärme von einem Kilogramm (1 kg) dieses Stoffes abgegeben oder aufgenommen wird, wenn sich seine Temperatur um ein Kelvin (1 K) ändert.
| Formelzeichen: | c |
| Einheit: | ein Kilojoule je Kilogramm und Kelvin |
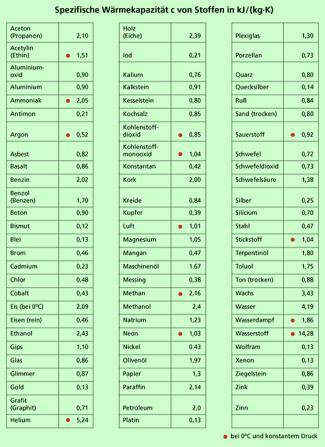
Die spezifische Wärmekapazität ist eine wichtige Stoffkonstante. In Bild 2 sind für die verschiedenen Stoffe die Werte für diese Stoffkonstante angegeben. Bei Gasen beziehen sich die angegebenen Werte auf konstanten Druck. Darüber hinaus gibt es für Gase auch eine spezifische Wärmekapazität bei konstanten Volumen.
-
Spezifische Wärmekapazität von Stoffen
Bedeutung der spezifischen Wärmekapazität von Wasser
Die Bedeutung der spezifischen Wärmekapazität von Wasser ergibt sich daraus, dass Wasser von allen in der Natur vorkommenden Stoffen mit die größte spezifische Wärmekapazität hat und darüber hinaus gut verfügbar ist. Der Wert von
bedeutet: Ein Liter Wasser nimmt eine Wärme von 4,19 kJ auf, wenn es um 1 K erwärmt wird. Es gibt eine Wärme von 4,19 kJ wieder ab, wenn es sich um 1 K abkühlt.
Große Wassermengen können demzufolge bei Temperaturänderungen große Mengen Wärme aufnehmen oder abgeben. Deshalb haben größere Seen, Meere oder Ozeane erheblichen Einfluss auf das Klima.
Im Frühjahr und Sommer wird vom Wasser bei Sonneneinstrahlung aufgrund der großen spezifischen Wärmekapazität des Wassers viel Wärme gespeichert. Diese Wärme wird auch der Umgebung entzogen. An großen Seen und Küsten ist es deshalb im Frühjahr und Sommer meist nicht so warm wie im Binnenland.
Im Herbst und Winter wird ein erheblicher Teil dieser Wärme an die Umgebung abgegeben. An großen Seen und Küsten ist es dann milder als im Binnenland. Durch große Wasserflächen entsteht somit ein typisches Seeklima mit relativ milden Wintern und relativ kühlen Sommern.
Beeinflusst wird das Klima in vielen Regionen auch durch gewaltige Meeresströmungen, z. B. durch den warmen Golfstrom, der seinen Ausgangspunkt im karibischen Raum (Mittelamerika) hat und der das Klima in England, Irland und an der norwegischen Küste deutlich beeinflusst.
Auch in der Technik besitzt Wasser wegen seiner großen spezifischen Wärmekapazität und natürlich auch wegen seiner guten Verfügbarkeit große Bedeutung. In Warmwasserheizungen wird genutzt, dass Wasser aufgrund seiner Wärmekapazität viel Energie durch Wärme transportiert. Für die Kühlung von Motoren oder als Kühlmittel in Kraftwerken wird aus diesem Grunde ebenfalls Wasser verwendet.
-
In Wasser ist viel thermische Energie gespeichert.


