Das Aufstellen chemischer Reaktionsgleichungen
Bei chemischen Reaktionen werden Stoffe umgewandelt. Es reagieren Ausgangstoffe zu Reaktionsprodukten. Dabei kommt es zum Umbau chemischer Bindungen, Teilchen ordnen sich neu an und Energieumwandlungsprozesse finden statt. Unterschiedliche Arten von Reaktionsgleichungen geben die qualitativen und die quantitativen Zusammenhänge der Stoffumwandlung wieder.
Eine chemische Reaktionsgleichung veranschaulicht mit Formeln, Symbolen und Zeichen die Prozesse bei einer chemischen Reaktion. Es gibt verschiedene Möglichkeiten der Darstellung von chemischen Reaktionsgleichungen:
1. Wortgleichungen,
2. Formelgleichungen und
3. Reaktionsschemata mit Strukturformeln.
Alle Arten von Reaktionsgleichungen sind nach dem gleichen Schema aufgebaut. Links vom Reaktionspfeil stehen die Ausgangsstoffe, die auch Reaktanten oder Edukte heißen. Rechts vom Reaktionspfeil stehen die Reaktionsprodukte, die auch als Endstoffe oder nur als Produkte bezeichnet werden.
![]()
1. Wortgleichung
| In einer Wortgleichung werden die reagierenden Stoffe mit ihren Namen angegeben. |
Aus einer Wortgleichung können nur die Ausgangsstoffe und die Reaktionsprodukte abgelesen werden. Die Stoffmengen und daraus resultierend die Massen der beteiligten Stoffe können aus ihr nicht abgeleitet werden.
Beispiel:
Wasserstoff kann mit Sauerstoff zur Reaktion gebracht werden.
Die Wortgleichung für diese chemische Reaktion lautet:
![]()
Sie wird wie folgt gelesen:
Wasserstoff und Sauerstoff reagieren zu Wasser.
Eine Wortgleichung kann in eine Formelgleichung umgewandelt werden.
-
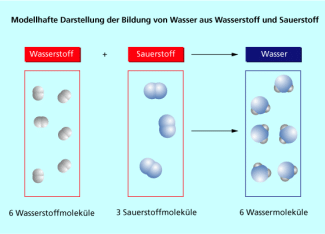
Modellhafte Darstellung der Bildung von Wasser aus Wasserstoff und Sauerstoff
2. Formelgleichung
| In einer Formelgleichung werden die reagierenden Stoffe mit ihren Formeln oder Symbolen dargestellt. Das Stoffmengenverhältnis der Ausgangsstoffe und der daraus gebildeten Reaktionsprodukte wird durch Stöchiometriezahlen angegeben. |
Bei chemischen Reaktionen reagieren die Teilchen immer in festen Zahlenverhältnissen miteinander, worüber Wortgleichungen nichts aussagen. Deshalb verwendet der Chemiker Formelgleichungen, in denen die reagierenden Teilchen mithilfe der chemischen Zeichensprache dargestellt werden. Die Stöchiometriezahlen vor den Formeln lassen quantitative Aussagen zum Stoffumsatz zu.
Beispiel:
Ein Wassermolekül besteht immer aus zwei Wasserstoffatomen und einem Sauerstoffatom. Daher muss bei der Reaktion von Wasserstoff und Sauerstoff zu Wasser das Verhältnis der reagierenden Teilchen folgendermaßen sein:
Ein anderes Zahlenverhältnis würde gegen das Gesetz von der Erhaltung der Masse verstoßen. Nach diesem Gesetz muss auf beiden Seiten des Reaktionspfeils die gleiche Anzahl von Atomen jeder Atomsorte stehen.Die Bildung von sechs Wassermolekülen aus sechs Wasserstoff- und drei Sauerstoffmolekülen ist in Bild 1 modellhaft dargestellt. Es reagieren immer zwei Wasserstoffmoleküle mit einem Sauerstoffmolekül. Daraus bilden sich zwei Wassermoleküle.
2 Wasserstoffmoleküle + 1 Sauerstoffmolekül → 2 Wassermolekülen.
Für die Reaktionspartner werden nun die Formeln oder Elementsymbole eingesetzt. Die Formelgleichung spiegelt das Zahlenverhältnis der reagierenden Teilchen bzw. das Stoffmengenverhältnis der Reaktanten wider:
2 H2 + O2 –→ 2 H2O
Beim Ermitteln der Stöchiometriezahlen bzw. Faktoren müssen die Gesetze der Erhaltung der Masse und der Ladung eingehalten werden. Eine allgemeine Schrittfolge zum Auftstellen der Formelgleichungen ist in Bild 2 angegeben. Diese Schrittfolge gilt für das Aufstellen vollständiger Formelgleichungen genauso wie für das Aufstellen verkürzter Ionengleichungen.Bei Gleichgewichtsreaktionen muss der Reaktionspfeil als Doppelpfeil dargestellt werden. Auf der Basis dieser Formelgleichungen können sämtliche stöchiometrischen Berechnungen durchgeführt werden.
-
Methode zum Aufstellen für einfache Reaktionsgleichungen


