Metallbindung
Die Metallbindung ist eine Art der chemischen Bindung, die durch Anziehungskräfte zwischen Metall-Ionen und freien Elektronen verursacht wird. Die meisten Metalle der Hauptgruppen besitzen nur wenige Außenelektronen, die leicht vom Metallatom abgegeben werden, da die Atomkerne auf die Außenelektronen nur geringfügige Anziehungskräfte ausüben. Dadurch entstehen positiv geladene Metall-Ionen und nahezu frei bewegliche Elektronen, die auch als Elektronengas bezeichnet werden.
Die meisten Metalle der Hauptgruppen besitzen nur 1 bis 3 Außenelektronen. Diese Außenelektronen der Metalle können leicht vom Metallatom abgegeben werden, da die Atomkerne auf die Außenelektronen nur geringfügige Anziehungskräfte ausüben. Dadurch entstehen positiv geladene Metall-Ionen und nahezu frei bewegliche Elektronen. Diese frei beweglichen Elektronen ermöglichen die gute elektrische Leitfähigkeit und die hohe Wärmeleitfähigkeit der Metalle.
Man bezeichnet die freien Elektronen im metallischen Festkörper auch als Elektronengas, weil sich die Elektronen wie Gasteilchen frei bewegen können. Mitunter nennt man das Elektronengas nach dem italienischen Physiker ENRICO FERMI (1901-1954) auch Fermigas. Das Elektronengas befindet sich zwischen den Metall-Ionen. Man spricht auch von einer Elektronengaswolke. Es handelt sich jedoch um eine Modellvorstellung.
-
Metallatome schwingen im Metallgitter um ihre Ruhelage.

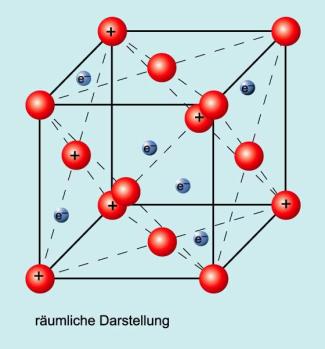
Die positiv geladenen Metall-Ionen (Atomrümpfe) und die Metallatome sind in einem Gitter, dem Metallkristall, regelmäßig angeordnet. Die abgespaltenen Elektronen bewegen sich in den Zwischenräumen frei und ungeordnet umher. Beim Anlegen eines elektrischen Stroms transportieren die Elektronen die Ladungen.
Steigt die Temperatur, dann verstärken sich die Schwingungen der Atomrümpfe im Gitter. Die Beweglichkeit des Elektronengases wird dadurch behindert und die elektrische Leitfähigkeit von Metallen sinkt.
Allerdings gilt dieses Modell nicht für Halbmetalle und andere Halbleiter. Deswegen wurde zur Beschreibung der Metallbindung ein leistungsfähigeres Modell, das sogenannte Bändermodell entwickelt, mit dem man auch die Eigeschaften der Halbmetalle erklären kann. Dieses ist in einem anderen Beitrag auf dieser CD beschrieben.
-
Die frei beweglichen Elektronen transportieren Ladungen im elektrischen Feld.