Organismen leben von freier Energie
Eine Zelle stellt ein energetisch offenes System dar. Ständig tauscht sie mit ihrer Umgebung Stoffe und Energie aus. Diesem Austausch liegen entsprechende physikalische Gesetzmäßigkeiten zugrunde. So erklären der 1. und 2. Hauptsatz der Thermodynamik die energetischen Verhältnisse in biologischen Systemen. Die Gesetze des Fließgleichgewichts gelten für alle biologischen Systeme und leiten sich aus der Nichtgleichgewichts-Thermodynamik her.
Thermodynamisches Gleichgewicht und freie Energie
Liegt eine chemische Reaktion vom Typ vor, stellt sich nach einer gewissen Zeit ein Gleichgewicht zwischen den Ausgangsstoffen A und B und den Endprodukten C und D ein. Seine Lage wird durch die thermodynamische Gleichgewichtskonstante K angegeben. Danach ist
K = c(C) x c(D) : c(A) x c(B),
wobei c(A) ... c(D) die Konzentrationen der Stoffe in Mol pro Liter darstellen, die sich im Gleichgewicht eingestellt haben. Je weiter die tatsächlichen Konzentrationen der Stoffe von den Gleichgewichtskonzentrationen entfernt sind, desto „energiereicher“ ist das System, d. h. desto mehr Energie wird bei der Reaktion zum chemischen Gleichgewicht hin freigesetzt.
Diese nutzbare freie Energie wird „freie Enthalpie“ genannt. Im Allgemeinen wird sie bei physiologischen Reaktionen für eine Temperatur von 25 °C, für einen Druck von 1 bar, einem Umsatz von 1 Mol und einem pH-Wert von 7 angegeben: . Die Maßeinheit ist .
Die Änderung der freien Enthalpie ist ein Kriterium dafür, ob eine Reaktion spontan verlaufen kann:
- Eine Reaktion kann nur spontan ablaufen, wenn negativ ist. Die Reaktion verläuft exergonisch.
- Ein System befindet sich im Gleichgewicht, wenn null ist.
- Eine Reaktion kann nicht spontan ablaufen, wenn positiv ist. Die Zufuhr von Energie ist notwendig, um die Reaktion anzutreiben. Die Reaktion verläuft endergonisch.
Fließgleichgewicht
Im Bild 1 wird das Fließgleichgewicht als hydraulisches Modell dargestellt: Es stellt sich z. B. beim abbauenden Stoffwechsel eines Organismus ein, bei dem ständig energiereiche Ausgangsstoffe (grau) zugeführt und energiearme Endprodukte (rot) abgeführt werden.
Durch ständigen Stoffaustausch mit der Umwelt wird verhindert, dass sich ein chemisches Gleichgewicht der einzelnen Reaktionen einstellt. Die Gleichgewichte der verschiedenen Teilreaktionen werden angestrebt, aber nie erreicht. Dadurch ist das Reaktionssystem zu dauernder Arbeitsleistung fähig. Das von der lebenden Zelle aufrechterhaltene Ungleichgewicht wird als Fließgleichgewicht bezeichnet. Eine lebende Zelle stellt damit ein energetisch offenes System dar. Sie steht mit ihrer Umwelt in einem ständigen Austausch von Stoffen und Energie. Theoretische Grundlage solcher Vorgänge ist nicht die klassische Thermodynamik, sondern die Nichtgleichgewichts-Thermodynamik. Aus ihr lässt sich ableiten, dass Leben nur fern vom thermodynamischen Gleichgewicht existieren kann. Trotz des Ungleichgewichtes liegen die verschiedenen Stoffe in annähernd konstanten Konzentrationen vor.
Prinzipiell gelten die Gesetzmäßigkeiten des Fließgleichgewichtes für alle biologischen Systeme auf allen Organisationsebenen:
- auf molekularer Ebene bei biochemischen Reaktionsketten der Stoffwechselwege,
- auf der Ebene der Organismen bei Stoffaustausch zwischen einzelnen Organen oder zwischen Organismus und Umwelt,
- auf der Ebene von Ökosystemen zwischen den Organismen.
-
Modell eines Fließgleichgewichts
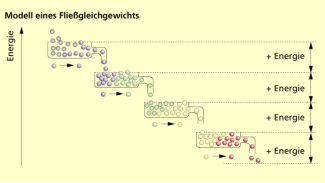
Die Abbildung stellt modellhaft eine einzelne Reaktion dar, z. B. Energie wird freigesetzt, solange das Ungleichgewicht besteht, brennt die Lampe. Ist das Gleichgewicht erreicht, wird keine Energie mehr freigesetzt, die Lampe erlischt.
Freie Enthalpie leistet Zellarbeit
- Mechanische Arbeit, z. B. Kontraktion von Muskelzellen.
- Transportarbeit, z. B. Transport von Molekülen durch Membranen entgegen dem Konzentrationsgefälle.
- Chemische Arbeit, z. B. Bildung von Makromolekülen aus Monomeren.
Bei der Zellatmung wird so lange Energie freigesetzt, so lange der Zelle Glucose und Sauerstoff zugeführt und Kohlenstoffdioxid und Wasser abgeführt werden. Um die Energie länger zur Verfügung zu haben, wird sie sofort als chemische Energie gebunden, meist als ATP.

