Plastom und Chondrom
Die genetische Information eines eukaryotischen Organismus ist vorwiegend in Form von DNA in den Chromosomen eines jeden Zellkerns lokalisiert. Außerdem enthalten Plastiden und Mitochondrien DNA und somit Erbinformation, und auch im Cytoplasma können Erbfaktoren vorliegen. Die Weitergabe solcher genetischen Informationen wird als extrachromosomale (außerhalb der Chromosomen stattfindende) Vererbung bezeichnet. Die Gesamtheit der Chromosomen-DNA heißt auch Genom, die DNA außerhalb des Zellkerns bildet das Plasmon. Nach der Unterscheidung von Plastiden- und Mitochondrien-DNA spricht man daher von Plastom als Gesamtheit der Gene aller Plastiden einer Zelle und Chondrom als Gesamtheit der Erbinformation aller Mitochondrien einer Zelle.
Grundlegend trägt die DNA von Mitochondrien und Plastiden zur Zellfunktion der Eukaryotenzelle bei. Besonders Enzyme des Energiestoffwechsels sind in ihnen codiert. Jedoch sind Mitochondrien und Plastiden nicht selbstständig lebensfähig, sondern funktionieren nur im engen Zusammenspiel mit dem Zellkern. Beispielsweise sind Teile der Mitochondrienmembran im Kern codiert und müssen erst in die Organellen transportiert werden.
Das Plastom
Die charakteristischen Organellen eukaryotischer Pflanzen sind Plastiden. Man unterscheidet Chloroplasten, Chromoplasten und Leukoplasten. Jede bestimmte Pflanzenzelle enthält jeweils nur einen bestimmten Plastidentyp. Die Hülle der Plastiden besteht aus jeweils einer inneren und einer äußeren Membran, der plasmatische Innenraum wird auch als Stroma oder Matrix bezeichnet. Im Stroma ist die ringförmige doppelsträngige DNA lokalisiert. Die Gesamtheit der DNA aller Plastiden einer Zelle nennt man Plastom.
Die Plastiden-DNA der meisten Pflanzen enthält nur wenig oder gar kein 5-Methyl-Cytosin. Dies hat zur Folge, dass die DNA beim Abkühlen nach Hitzeeinwirkung (90 °C) auf die Temperatur von 60 °C schnell und nahezu vollständig renaturiert. Dies ist ein wichtiges Unterscheidungsmerkmal zur Kern-DNA, die diesen Prozess wesentlich langsamer und unvollständig durchläuft.
Eine Pflanzenzelle verfügt über 50-100 Plastiden, wobei jeder Chloroplast etwa 10-20 Nucleoide beinhaltet. Diese bestehen ihrerseits aus 5-10 DNA-Molekülen. Insgesamt sind also bis zu 10 000 Plastiden-DNA-Moleküle pro Zelle nachweisbar. Die Größe der einzelnen DNA-Moleküle variiert bei den einzelnen Spezies zwischen 70 kb und etwa 300 kb.
Sowohl genetisch als auch stoffwechselphysiologisch können Plastiden als semiautonome (halbselbstständige) Zellorganellen eingestuft werden. Ihre DNA codiert für eine Reihe von für den Plastiden wichtigen Proteinen. Die nachstehende Übersicht vermittelt auszugsweise einen Eindruck über die von der Plastiden- DNA codierten Gene bei Sprosspflanzen.
| Gene | Proteine |
| Fotosynthese-Gene | Elektronentransport |
| ATP-Synthase | |
| große Untereinheit Rubisco | |
| Fotosystem I und II | |
| Gene für plastidäre Ribosomen | ribosomale RNA |
| ribosomale Proteine | |
| Gene für plastidäre tRNAs | |
| Gene für plastidäre NADH- Dehydrogenase | |
| Gene für Replikation, Transkription und Translation | RNA-Polymerase |
| Initiationsfaktor IF-1 |
-
Der genetische Apparat der Pflanzenzelle
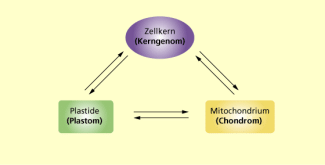
Zusammenwirken von Genotyp und Plastom
Voll ausdifferenzierte und funktionstüchtige Chloroplasten können nur durch das Zusammenwirken von Kern-Genen und Plastiden-Genen entstehen. Dies resultiert daraus, dass nur ein Teil der im Plastiden benötigten Proteine vom Plastom codiert wird und der andere Teil vom Genom (Zellkern).
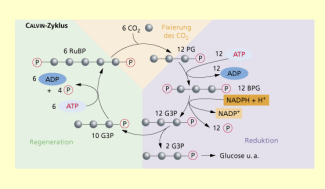
Am Beispiel eines Enzyms kann sehr anschaulich die Interaktion zwischen chromosomalem Erbgut des Zellkerns und des Plastoms dargestellt werden. Das Enzym, das den ersten Schritt des CALVIN-Zyklus katalysiert, Ribulose-1,5-bisphosphat-Carboxylase im Folgenden kurz Rubisco genannt, ist aus mehrfacher Sicht bemerkenswert. Es ist das häufigste Protein in den Chloroplasten und vermutlich auch weltweit das in den größten Mengen vorhandene Protein. Die Carboxylase ist verantwortlich für die CO2-Bindung während der Fotosynthese und kommt daher in den grünen Blättern der Pflanzen in großen Mengen vor.
Die quartäre Struktur dieses Eiweißmoleküls setzt sich aus einer großen und einer kleinen Untereinheit zusammen. Die oben stehende Übersicht zeigt, dass nur das Polypeptid für die große Untereinheit auf dem Plastom codiert ist, das Gen für die kleine Untereinheit dagegen ist im Zellkern verschlüsselt, folgt den mendelschen Regeln und wird durch die plasmatischen Ribosomen translatiert. Die Synthese der Untereinheit findet im Cytoplasma der Zelle statt, von wo aus anschließend ein Transport in die Chloroplasten erfolgt. Das vollständige Enzym Rubisco wird im Stroma des Chloroplasten gebildet. Das heißt die Untereinheiten der plastidären Proteinkomplexe werden zum Teil vom Kern und zum Teil vom Plastom codiert. Plastiden sind also nicht vollends eigenständig (hemiautonom).
Transkription im Plastom
Plastiden besitzen ein eigenes Proteinsynthesesystem. Bei der Realisierung der genetischen Information des Plastoms sind die Analogien zum Genom der Einzeller besonders auffällig. So entspricht die ribosomale DNA der Plastiden eher dem Bakterientyp E. coli als der eigenen Kern-DNA. Des Weiteren begegnet uns in der Plastiden-DNA eine Operon-ähnliche Anordnung der Gene. Allerdings werden einzelne Polymerasen auch kerncodiert, wobei die Transkription ein typisches Merkmal der vielzelligen Organismen ist.
Im Verlauf der Prozessierung (Reifung) der RNA werden zunächst aus einer Vorläufer-RNA (prä-RNA) Stücke (Intronen) herausgeschnitten. Dann werden mehrere RNA-Moleküle einzeln transkribiert, die danach zu einem vollständigen RNA-Molekül zusammengefügt werden.
Da, wie schon angesprochen, Enzym-Untereinheiten zum Teil vom Kerngenom und zum Teil vom Plastom codiert werden, ist eine enge Koordinierung der Genexpression nötig. Dies wird durch Regulation der Transkription und eine spezifische RNA-Stabilität garantiert.
-
Calvin-Zyklus
Plastidentransformation
Im Rahmen der genetischen Optimierung von Nutzpflanzen wurden neben der Kerntransformation auch schon direkte und dauerhafte Veränderungen des Informationsgehalts des Plastoms realisiert. Zum Einsatz kam hier u. a. die sogenannte biolistische Transformation. Hierbei werden Goldkügelchen mit DNA beschichtet und in die Zelle geschossen. Dabei gelangt DNA in die Plastiden. Mittels eines Resistenzgens kann man dann Pflanzen mit transformierten Plastiden selektieren, die dann beispielsweise einen höheren Eiweißgehalt aufweisen.
Erfolgreich wurde diese Methode bislang bei Tabak, Reis und Tomate praktiziert, besonders bei Tabak wurden bereits verschiedene Gene erfolgreich transformiert. Einen Vorteil gegenüber der Kerntransformation weist die Plastidenvererbung in dem Punkt auf, dass keine unkontrollierte Verbreitung der gentechnisch veränderten Pflanzen über den Pollen erfolgt (da Chloroplasten nur mütterlicherseits vererbt werden) und somit keine direkte Gefährdung der ökologischen Sicherheit besteht.
Das Chondrom
Die zweiten Zellorganellen, die neben dem Zellkern noch Erbmaterial enthalten, sind die Mitochondrien. Sie gehen durch Teilung auseinander hervor und können zunächst als Promitochondrien vorliegen, die sich durch Sauerstoffanwesenheit in „echte“ Mitochondrien umwandeln. Diese besitzen die typische Doppelmembranstruktur, bei der sich die Innenmembran in verschiedene Gebilde faltet (Cristae, Sacculi, Tubuli). In deren Wandungen sind die Elemente der Atmungskette enthalten.
Mitochondrien haben eine zentrale Stellung im Zellstoffwechsel. So sind in ihnen die Enzyme der Atmungskette lokalisiert und u. a. ist der Citratzyklus an diese Organellen gebunden. Die Anzahl der Mitochondrien pro Zelle ist um ein Wesentliches höher als die der Plastiden – sie kann bis zu 700 sein.
Die Gesamtheit der Erbsubstanz aller Mitochondrien einer Zelle bezeichnet man als Chondrom. Ähnlich wie beim Plastom existieren hinsichtlich der Organisation große Übereinstimmungen zu den Einzellern. Beide gelten als Relikte des Genoms eines Endosymbionten, z. B. stammesgeschichtliche Ahnen der α-Purpurbakterien im Falle des Chondroms (Symbiontenhypothese). Diese Erklärung beruht auf der Tatsache, dass im Laufe der Evolution eukaryotische Zellen prokaryotische Elemente in sich aufgenommen und für sich nutzbar gemacht haben. Aus diesem Grund besitzen Chloroplasten und Mitochondrien ein eigenes funktionstüchtiges Genom, das dem Genom eines Einzellers mehr gleicht als dem eines vielzelligen Organismus.
Im Gegensatz zur noch relativ unbekannten molekularen Struktur des Plastoms ist diese bei der mitochondrialen DNA weitestgehend aufgeklärt und detailliert analysiert. Sie enthält ca. 40 Gene, während die um ein Wesentliches längere Plastom-DNA bis zu 200 Gene beinhaltet. Die DNA ist doppelsträngig und ringförmig oder linear (Grünalge Chlamydomonas). Oft ist die Mitochondrien-DNA verdrillt. Sie unterscheidet sich von der Kern-DNA ähnlich wie die Plastiden-DNA durch ihr Renaturierungsverhalten, und zwar renaturiert auch sie schneller und vollständiger zur Ausgangsstruktur als die Kern-DNA. Die Anwendung von Restriktionsenzymen und Deletionen ermöglichte eine molekulargenetische Kartierung der Mitochondrien-DNA. So konnte bereits 1980 von der Forschungsgruppe um FREDERICK SANGER (*1918) die gesamte Nucleotidsequenz der Mitochondrien-DNA des Menschen aufgeklärt werden – das menschliche Mitochondrien-Chromosom besteht aus 16 569 Basenpaaren (bp).
Bezüglich der Größe der Mitochondrien-DNA existieren gravierende Unterschiede. Die nachfolgende Übersicht zeigt die teilweise enormen artspezifischen Abweichungen im Speicherumfang des Chondroms.
| Art | Größe [kb] |
| Homo sapiens (Mensch) | 16,6 |
| Paramecium aurelia (Pantoffeltierchen) | 40,5 |
| Saccharomyces cerevisiae (Bierhefe) | 68,0-81,0 |
| Marchantia polymorpha (Brunnenlebermoos) | 186,6 |
| Arabidopsis thaliana (Acker-Schmalwand) | 366,9 |
| Citrullus lanatus (Wassermelone) | 330 |
| Cucumis melo (Melone) | ca. 2 400 |
-
An der Tabakpflanze glückte die Genübertragung.

Nur wenige Gene werden mitochondrial codiert, die nachfolgende Übersicht vermittelt einen exemplarischen Eindruck für das Brunnenlebermoos.
| Funktionsbereich | Anzahl der Gene |
| Translation: | |
| – rRNAs | 3 |
| – tRNAs | ~29 |
| – ribosomale Proteine | 16 |
| Atmungskette: | |
| – NADH-Dehydrogenase | 7 |
| – Cytochrom-b/c-Komplex | 1 |
| – Cytochrom-c-Oxidase | 3 |
| – ATP-Synthase | 3 |
Auch hier erkennt man, dass die Großorganellen die Grundstrukturen für ihre 70 S Ribosomen im eigenen Erbspeicher verschlüsseln. Jedoch beträgt dieser Eigenanteil lediglich 5 %. Die große Mehrheit der mitochondrialen Proteine wird im Zellkern codiert, im Cytoplasma synthetisiert und anschließend in die Organellen transportiert.
Seit Mitte der 80er-Jahre ist bekannt, dass Mutationen der Mitochondrien Krankheiten verursachen können. Dazu zählen beispielsweise das Leber-Syndrom, neurogene Muskelschwäche oder Atmungsdefekte. Sogar eine Antibiotikaresistenz kann als Folge von Mitochondrienmutationen auftreten.

