Aminosäuren
Aminosäuren sind organische Verbindungen, die über mindesten je ein Amino-Gruppe und mindestens eine Carboxy-Gruppe im Molekül verfügen. Die in der Natur am häufigsten vorkommenden Aminosäuren sind die -Aminosäuren. 22 dieser Verbindungen werden als biogene oder proteinogene Aminosäuren bezeichnet, da aus sie die Bausteine der Proteine sind. Aminosäuren liegen in einer zwitterionischen Struktur vor und verhalten sich wie Ampholyte. Die Moleküle können weitere funktionelle Gruppen enthalten, die die Stoffeigenschaften bestimmen.
Aminosäuren sind organische Verbindungen, die über mindestens eine Amino-Gruppe und mindestens ein Carboxy-Gruppe verfügen. In Abhängigkeit der Stellung der Amino-Gruppe zum Kohlenstoffatom der Carboxy-Gruppe unterscheidet man -, -, - und -Aminosäuren (Bild 1). Viele der in der Natur vorkommenden Aminosäuren verfügen über weitere funktionelle Gruppen. Man kennt heute ca. 500 natürliche Aminosäuren. Dabei sind die am Aufbau der Proteine beteiligten -Aminosäuren besonders wichtig; sie kommen am häufigsten in der Natur vor. Als erste frei in der Natur vorkommende Aminosäuren wurde 1806 das Asparagin von VAUQUELIN und ROBIQUET aus dem Saft von Spargelpflanzen (Asparargus) entdeckt und isoliert.
-
Bei Aminosäuren kann die Stellung der Aminogruppe unterschiedlich sein. Danach werden sie zunächst eingeteilt.
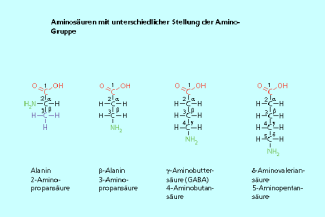
Nomenklatur
Die in der Natur vorkommenden -Aminosäuren werden mit Trivialnamen bezeichnet. Die Bezeichnung richtet sich dabei im Wesentlichen nach dem ursprünglichen Protein, aus dem die Aminosäure zum ersten Mal isoliert wurde z. B. Asparagin aus Spargelsaft (lat: asparagus = Spargel), Serin aus Seide (griech: seros = Seidenraupe), Cystein aus Blasensteinen (griech: cystis = Blase), Tyrosin aus Käse (griech.: tyros = Käse). Einige Namen von Aminosäuren beruhen auch auf strukturellen Ähnlichkeiten der Aminosäure zu anderen Naturprodukten z. B. Threonin zum Monosaccharid Threose, Valin zur iso-Valeriansäure (3-Methylbutansäure).
Die -Aminosäuren unterscheiden sich untereinander nur im Rest R am -Kohlenstoffatom. Dieser Rest wird als Seitenkette bezeichnet.
Reaktivität von Aminosäuren
Das Stickstoffatom der Amino-Gruppe ist ein basisches Zentrum, denn es verfügt über ein freies Elektronenpaar. Im Gegensatz dazu besitzt die Carboxy-Gruppe saure Eigenschaften. Folglich sind zwei funktionelle Gruppen in einem Molekül enthalten, die eine entgegensetzte Reaktivität haben.
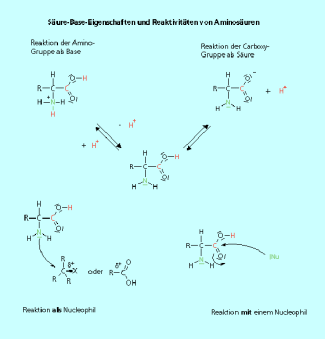
Aufgrund ihres bifunktionellen Charakters sind Aminosäuren Ampholyte. Das heißt, sie können sowohl als BRÖNSTED-Base (Aufnahme eines Protons) als auch als BRÖNSTED-Säure (Abgabe eines Protons) reagieren (Bild 2). Anders als bei dem Ampholyten Wasser sind das saure und das basische Zentrum durch Kohlenstoffatome getrennt.
Außerdem können Aminosäuren sowohl mit Nucleophilen als auch mit Elektrophilen reagieren. Auf diese Weise verbinden sich beispielsweise mehrere Aminosäuren zu Peptiden: Die Amino-Gruppe fungiert als nucleophiles Zentrum, die Carboxy-Gruppe als elektrophiles Zentrum.
-
Die Amino-Gruppe ist basich, die Carboxy-Gruppe sauer. Aminosäuren sind also Ampholyte und reagieren sowohl mit Säuren als auch mit Basen. Auch bei Substitutionsreaktionen zeigt sich der bifunktionelle Charakter.
Die α-Aminosäuren
- Biogene Aminosäuren
Die -Aminosäuren nehmen eine Sonderstellung ein. Sie werden häufig als die Bausteine des Lebens bezeichnet. Die -Aminosäuren sind die Bausteine der Proteine und Polypeptide. Bei allen Lebewesen werden 22 dieser -Aminosäuren in der DNA/RNA codiert. Das heißt, zum allergrößten Anteil enthält unsere DNA den Bauplan für die Primärstruktur von Polypeptiden und Proteinen. Diese Aminosäuren werden als proteinogene oder biogene Aminosäuren bezeichnet (Bild 3).
-
Diese 22 biogenen Aminosäuren sind die Bausteine der Proteine.
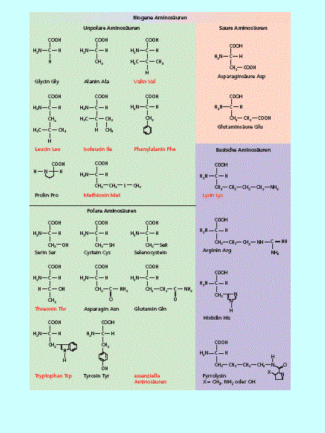
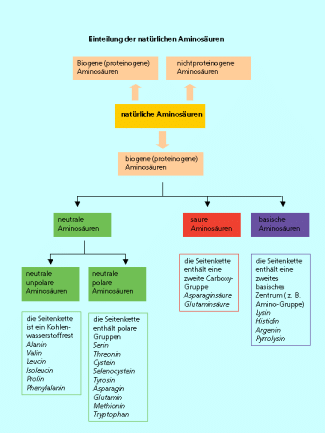
Sie werden unterteilt in neutrale, saure und basische Aminosäuren (Bild 4). Saure Aminosäuren haben eine zweite Carboxy-Gruppe, basische Aminosäuren haben außer der Amino-Gruppe am -Kohlenstoffatom mindestens ein weiteres Stickstoffatom. Mit Ausnahme der kleinsten biogenen Aminosäure, dem Glycin, haben alle -Aminosäuren am -Kohlenstoffatom ein Chiralitätszentrum. In die natürlichen Proteine werden nur die L--Aminosäuren eingebaut.
In einigen Fällen findet man in bestimmten Proteinen auch andere Aminosäurereste. Diese veränderten Aminosäurereste stammen aus ursprünglich proteinogenen Aminosäuren, die nach dem Einbau in Proteine an der Seitenkette verändert worden sind (posttranslationelle Modifikation). Sie haben wichtige Funktionen in Enzymen und Hormonen.
-
Die natürlichen Aminosäuren werden nach der Polarität der Moleküle unterteilt.
Drei- und einbuchstabige Abkürzungen der Aminosäuren
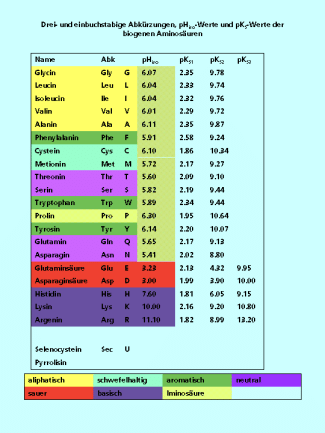
Für die biogenen Aminosäuren gibt es eine dreibuchstabige Abkürzung. Dabei werden häufig die ersten drei Buchstaben des Namens benutzt z. B. Alanin = Ala, Cystein = Cys, Phenylalanin = Phe. Ausnahmen bilden Aspargin = Asn und Glutamin = Gln, um sie von der Asparaginsäure = Asp und der Glutaminsäure = Glu zu unterscheiden. Auch beim Tryptophan = Trp wird von dieser Regel abgewichen um Verwechslungen mit dem Tyrosin = Tyr zu vermeiden. Seltener – vor allem von Biochemikern – wird eine einbuchstabige Abkürzung verwendet (Bild 5).
-
Isoelektrische Punkte, pKs-Werte und Codierung der 22 biogenen Aminosäuren
Nichtproteinogene Aminosäuren
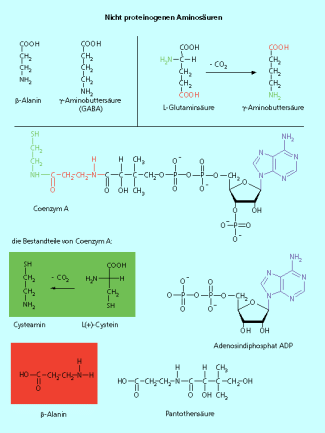
Nichtproteinogene Aminosäuren sind zwar nicht Bestandteile der Eiweiße, erfüllen aber trotzdem wichtige Funktionen im Organismus. Immerhin mehr als 250 Vertreter sind bisher im Organismus nachgewiesen worden. Dazu gehören z. B. das -Alanin und die -Aminobuttersäure. Das -Alanin ist Bestandteil des Coenzyms A , die -Aminobuttersäure (engl.: -Amino-butyric acid GABA) ist ein wichtiger Neurotransmitter (Bild 6). Das für das Coenzym A notwendige -Alanin wird vom Menschen aus dem Vitamin B-Komplex aufgenommen.
-
Strukturformeln der nichtproteinogenen Aminosäuren beta-Alanin und GABA sowie von Coenzym A, das unter anderem beta-Alanin enthält
Der isoelektrische Punkt
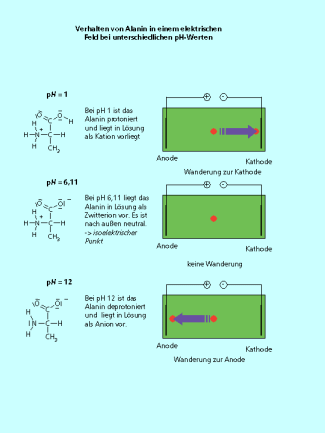
Bringt man Aminosäuren (z. B. in einer Lösung oder einem Gel) in ein elektrisches Feld, dann bewegen sich die Teilchen – je nach ihrer Ladung – in Richtung Anode oder Katode. Die Ladung der Teilchen wird durch den amphoteren Charakter des Moleküls und den pH-Wert der Lösung bestimmt. Im stark sauren pH-Bereich ist die Amino-Gruppe protoniert, und die Aminosäure liegt als Ammonium-Kation vor. Im stark basischen pH-Bereich wird dagegen die Carboxy-Gruppe deprotoniert, sodass Carboxylat-Anionen gebildet werden, die zur Anode wandern (Bild 7).
Im dazwischen liegenden pH-Bereich bilden die Aminosäureteilchen sogenannte Zwitterionen, d. h. die Amino-Gruppe ist positiv und die Carboxy-Gruppe negativ geladen. In der Summe heben sich die beiden Ladungen auf, das Zwitterion ist insgesamt elektrisch neutral. Die Zwitterionen liegen im Gleichgewicht mit den Ammonium-Kationen und Carboxylat-Anionen vor. Die Lage der Gleichgewichte ist abhängig vom pH-Wert der Lösungen.
Bei einem bestimmten pH-Wert ist der Anteil der Zwitterionen einer Aminosäure maximal. Da diese Teilchen insgesamt neutral sind, bewegen sie sich im elektrischen Feld weder in die eine noch in die andere Richtung. Der entsprechende pH-Wert wird der isoelektrische Punkt der Aminosäure genannt (Bild 7). Er hängt vom Bau der Aminosäuren ab und liegt bei unterschiedlichen pH-Werten.
Am isoelektrischen Punkt ist nicht nur die Leitfähigkeit der Lösung sehr gering. Auch die Löslichkeit der Aminosäuren ist am isoelektrisch Punkt minimal, weil die Teilchen insgesamt neutral und damit am wenigsten polar sind.
-
Die Ladung der Aminosäureteilchen bestimmt ihre "Wanderungsrichtung" im elektrischen Feld. Am isoelektrischen Punkt ist das Zwitterion insgesamt neutral und wandert deshalb nicht.
Nachweisreaktionen der Aminosäuren (Farbreaktionen)
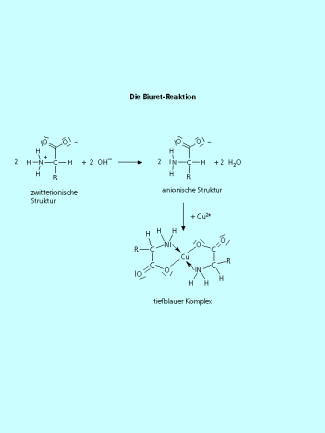
Bei der BIURET-REAKTION (Bild 8) wird die Ausbildung von Komplexen der Aminosäuren mit Kupfer(II)-Ionen in alkalischer Lösung ausgenutzt. Es entstehen tiefblau bis violett gefärbte Lösungen. Auch Eiweiße geben die gleiche Reaktion. Nach einer entsprechenden Kalibration kann die Reaktion sogar zur quantitaven Eiweißbestimmung mithilfe eines Fotometers benutzt werden.
-
In der Biuret-Reaktion bilden Aminosäuren nach der Deprotonierunhg mit einer Base mit Cu(II)-Kationen einen tiefblau bis violett gefärbten Komplex.
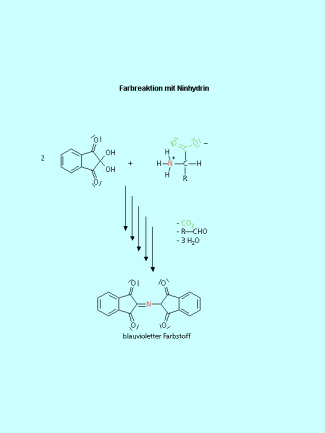
Aminosäuren reagieren mit Ninhydrin unter Ausbildung eines blauvioletten Farbstoffes. Bei dieser Reaktion wird das Stickstoffatom der Aminosäuren übertragen. Der gebildete Farbstoff besteht aus zwei Ninhydrin-Einheiten, die über ein Stickstoffatom verbunden sind (Bild 9). Die Reaktion verläuft über mehrere Stufen. Sie beginnt mit der Decarboxylierung der Aminosäure. Es folgt ein Angriff des Stickstoffatoms auf das Kohlenstoffatom des Ninhydrins.
-
Mit Ninhydrin bilden Aminosäuren einen blauviolett gefärbten Komplex. Zur Bildung diese Komolexes wird in komplizierter Reaktionsabfolge das Stickstoffatom der Aminosäure verwendet.
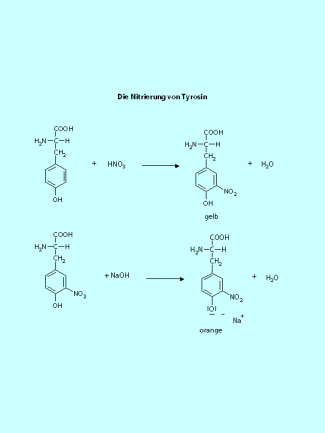
Die Aminosäure Tyrosin regiert mit konzentrierter Salpetersäure (Bild 10). Es entsteht eine gelbe Lösung. Wird das Reaktionsprodukt mit Ammoniak-Lösung alkalisch gemacht, beobachtet man eine Farbvertiefung nach dunkelorange. Der Phenolring wird durch die Salpetersäure nitriert, die Farbvertiefung resultiert aus der Deprotonierung der sauren phenolischen Hydroxy-Gruppe. Diese Reaktion ist auch die Grundlage der XANTHOPROTEIN-REAKTION als Nachweis-Reaktion für Eiweiße.
Synthetische Aminosäuren im Alltag
Neben den Aminosäuren, die bei biochemischen Prozessen und bei der Proteinsynthese von großer Bedeutung sind, begegnen uns im Alltag auch synthetisch hergestellte Aminosäuren.
Glutamat als Geschmacksverstärker
Entgegen einer lange vertretenen Hypothese, dass die menschliche Zunge nur vier unterschiedliche Geschmacksrichtungen wahrnehmen kann, stellten japanische Wissenschaftler fest, dass wir mindestens über einen fünften Geschmackssinn verfügen. Dieser Geschmackssinn heißt Umami (eine Übersetzung ist schwierig, wir müssten dazu "fleischig" oder "aminosäurig") sagen. Die japanische Gruppe konnte nachweisen, dass unsere Geschmackszellen Rezeptoren haben, die bestimmte Aminosäuren wie die Glutaminsäure (der Geschmacksverstärker Glutamat ist das Natriumsalz der Glutaminsäure) erkennen. Bei dieser Erkennung wird ein Botenstoff ausgesandt, der eine Signalübermittlung an das Gehirn erzeugt.
-
Auf dem gleichen Reaktionsprinzip wie die Nitrierung von Tyrosin beruht die Xanthoprotein-Reaktion, die als Nachweis für Eiweiße dient.
Aminosäure-Derivate als Süßstoffe
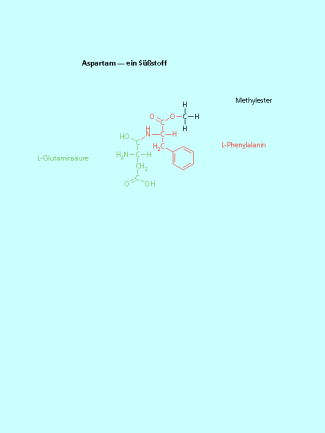
Diabetiker müssen den Konsum von Kohlenhydraten stark einschränken. Deshalb wurden Süßstoffe entwickelt, die nicht auf der Basis von -Glucose-Einheiten einen süßen Geschmack erzeugen. Ein Beispiel ist das Aspartam, dass eine 200-fache Süßkraft gegenüber von Rohrzucker besitzt (Bild 11). Aspartam ist ein Dipetid aus L-Asparaginsäure und L-Phenylalanin. Die Peptidbindung wird gebildet aus der Amino-Gruppe des Phenylalanins und der Carboxy-Gruppe der Asparginsäure am -Kohlenstoffatom. Die Carboxy-Gruppe des Phenylalanins wurde verestert, die zweite Carboxy-Gruppe der Asparaginsäure bleibt unverändert.
-
Der Süßstoff Aspartam besitzt die 200-fache Süßkraft von gewöhnlichem Haushaltszucker (Rohrzucker ).
ACC-akut bei Husten
Im ACC-akut befindet sich eine veränderte Aminosäure, das Acetylcystein. Das Acetylcystein ist ein starkes Reduktionsmittel. Es ist in der Lage, Disulfidbrücken zu spalten. Der menschliche Schleim enthält sehr viele Disulfidbrücken. Durch die Spaltung dieser Disulfidbrücken, sinkt die Viskosität des Schleimes. Er wird dadurch "dünnflüssiger". Das erleichtert ein Abhusten der schleimigen Sekrete. Deshalb empfiehlt der Arzt bei Erkältungskrankheiten mit starker Schleimbildung die Einnahme von ACC-akut. Das Acetylcystein entsteht bei der Umsetzung von Cystein mit einem Essigsäurederivat. Dabei wird ein Carbonsäureamid gebildet. In der Technik muss Essigsäurechlorid oder Essigsäureanhydrid benutzt werden, da mit der freien Essigsäure nur eine Säure-Base-Reaktion stattfindet.
Suche nach passenden Schlagwörtern
- Threonin
- Eiweisse
- GABA
- Coenzym A
- Peptide
- Tryptophan
- Asparagin
- ACC
- Valin
- Eieweiße
- Leucin
- Hormone
- biogene
- Serin
- ACC-akut
- Asparaginsäure
- Glutamat
- Proteine
- Enzyme
- Biuret-Reaktion
- Zwitterion
- Süßstoff
- Aspartam
- Alanin
- Cystein
- Phenylalanin
- N-Terminus
- Xanthoprotein-Reaktion
- Glutamin
- Ninhydrin
- isoelektrischer Punkt
- pH-Wert
- Seitenkette
- Glycin
- proteinogene Aminosäuren
- Glutaminsäure
- Acetylcystein

