Physikalische Grundlagen der Farbigkeit
Menschliche Augen können den Teil des elektromagnetischen Lichts wahrnehmen, der als sichtbares Licht oder VIS-Bereich bezeichnet wird und Wellenlängen zwischen 400 und 800 nm aufweist.
Chemische Verbindungen erscheinen farbig, wenn sie eine bestimmte Wellenlänge aus diesem Bereich absorbieren, sie zeigen dann die Komplementärfarbe der absorbierten Wellenlänge.
Weshalb es zur Absorption von Licht bestimmter Wellenlängen kommt, lässt sich mithilfe der Molekülorbital-Theorie erklären.
Das menschliche Auge ist in der Lage, einen bestimmten Bereich elektromagnetischer Wellen, das sichtbare Licht , wahrzunehmen. Er liegt zwischen 400 nm und 800 nm und wird VIS-Bereich genannt. Jede Wellenlänge entspricht einer bestimmten Farbe, die wir sehen, und einer bestimmten Energie.
Schickt man weißes Sonnenlicht durch ein Prisma, stellt man fest, dass es sich aus vielen Farben, den Spektralfarben, zusammensetzt. Umgekehrt lassen sich die Spektralfarben mit Hilfe einer Sammellinse wieder zu weißem Licht vereinigen.
Ein Prisma in der Natur sind Wassertropfen: Scheint Sonnenlicht durch Regentropfen, entsteht ein Regenbogen.
Dass uns Stoffe farbig erscheinen, liegt an der Fähigkeit dieser Verbindungen, Licht einer bestimmten Wellenlänge im VIS-Bereich zu absorbieren. Der nicht absorbierte Teil des Lichts, also die Komplementärfarbe ist sichtbar.
![]()
Dieses Phänomen lässt sich mit Hilfe der Molekülorbital-Theorie erklären. Die kovalenten Bindungen in einem Molekül entstehen jeweils durch die Bildung energiearmer bindender Molekülorbitale (MOs) und dazugehöriger antibindender Molekülorbitale höherer Energie.
Da die antibindenden MOs nicht oder nicht vollständig mit Elektronen besetzt sind, können Elektronen aus den tiefer liegenden Orbitalen in antibindenden MOs übergehen, indem sie genau das dafür nötige Energiequantum absorbieren, d. h. Licht derjenigen Wellenlänge, die dieser Energie entspricht.
-
Die Energiemengen, die für den Elektronenübergang in antibindende MOs nötig sind, und damit die Wellenlänge des absorbierten Lichts, hängen von der Art der beteiligten MOs, d. h. von der Struktur der Verbindung ab.

Die Energie, die nötig ist, um solche Elektronenübergänge zu ermöglichen, und damit die erforderliche Wellenlänge der absorbierten Strahlung werden von der Struktur der chemischen Bindungen bestimmt. So ist die benötigte Energie unterschiedlich, je nachdem, ob es sich um Einfach-, Doppel- oder Dreifachbindungen handelt. Für den Elektronenübergang in einer Einfachbindung ist erheblich mehr Energie nötig als für einen in einer (Doppel- oder Dreifachbindung) oder einem von einem nicht bindenden MO eines freien Elektronenpaars in ein antibindendes MO (Bild 2).
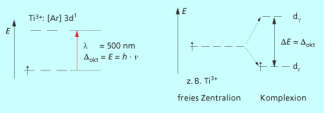
Die Farbigkeit der Komplexverbindungen der Nebengruppenelemente beruht darauf, dass die entarteten d-Orbitale unter dem Einfluss beispielsweise eines oktaedrischen Ligandenfelds aufspalten (Bild 3). Die Energiedifferenz ΔE liegt im Bereich des sichtbaren Lichts. Die Farbe des purpurroten Ti(H2O)6 3+-Komplexes resultiert aus der Anregung des d-Elektrons in das höhere Niveau mit dem Absorptionsmaximum bei 500 nm.
-
Die Farbigkeit der Komplexverbindungen der Nebengruppenelemente beruht darauf, dass die entarteten d-Orbitale unter dem Einfluss des Ligandenfelds aufspalten.