Säure-Base-Titration
Eine einfache und trotzdem sehr zuverlässige Methode der quantitativen Analyse ist die Titration, die schon sehr lange zur Bestimmung der Konzentration wässriger Lösungen angewendet wird. Das Grundprinzip besteht darin, zu einer Analysenlösung unbekannter Konzentration eine Maßlösung eines Stoffes bekannter Konzentration zu geben. Wenn beide Stoffe vollständig miteinander reagieren, kann aus dem Volumen der Maßlösung die Konzentration der Analysenlösung berechnet werden. Dieses Prinzip kann sowohl bei Säure-Base-Reaktionen als bei auf anderen Reaktionstypen zur quantitativen Analyse genutzt werden.
Säure-Base-Titrationen kommen vielfältig zum Einsatz: für die Überwachung von Umweltprozessen, wie die Analyse der Wasser- und Bodenqualität, aber auch bei der Herstellung von Lebens- und Arzneimitteln.
Die rasante Entwicklung des Wissens in den Natur- und Gesellschaftswissenschaften stellt uns alle vor täglich neue Fragen. So vergeht kaum ein Tag, an dem in der Kriminalistik nicht nach Spuren körpereigener Substanzen und Gifte, in der Umweltforschung nach Verunreinigung in Luft und Wasser, in der Medizin nach unseren Körper steuernden oder schädigenden Substanzen gefahndet wird. Besonders in Lebensmitteln und Haushaltschemikalien wie Reinigungsmitteln sind unterschiedliche Säuren und Basen enthalten. Der Säuregehalt ist für den Geschmack und die Haltbarkeit der Lebensmittel und die Reinigungswirkung eines Entkalkers von entscheidender Bedeutung und wird daher ständig von den Herstellern kontrolliert. Die analytischen Methoden dafür werden immer ausgefeilter, sicherer, aussagekräftiger und genauer.
Dabei interessiert die Auftraggeber neben der Frage: „Was ist in den Proben vorhanden?“ (Frage nach der Qualität), vor allem auch „Wie viel ist davon enthalten?“ (Frage nach der Quantität).
Eine einfache und trotzdem sehr zuverlässige Methode der quantitativen Analyse ist die Titration, die schon sehr lange zur Bestimmung der Konzentration wässriger Lösungen angewendet wird. Die Bezeichnung leitet sich aus dem Französischen begriff für Gehalt her (franz.: titre = Gehalt).
Prinzip der Titration
Man geht bei Titrationen von folgendem Grundprinzip aus:
1. Ein genau abgemessener Teil der zu untersuchenden Probe wird in einem genau definierten Volumen Lösungsmittel (meist Wasser) gelöst. Die so erhaltene Analysenlösung enthält nun den Titranten, d. h. den zu bestimmenden Stoff.
2. Zu dieser Analysenlösung wird unter Rühren oder Schütteln durch langsames und vorsichtiges Zutropfen eine Maßlösung (Lösung mit bekannter Konzentration) gegeben, die den Titrator enthält.
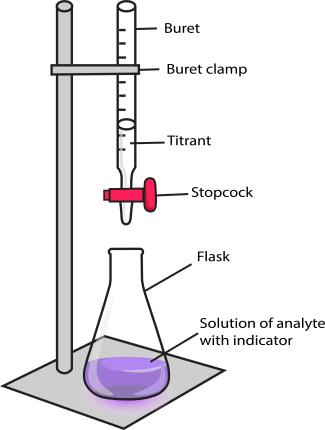
3. Die beiden Lösungen reagieren miteinander in einer bekannten Reaktion. Das Zutropfen der Maßlösung zur Analysenlösung geschieht mithilfe einer Bürette solange bis der Äquivalenzpunkt der Reaktion erreicht ist.
Der Äquivalenzpunkt ist der Punkt, an dem die Menge des Titranten genau der Menge des Titrators äquivalent ist (also beide so miteinander reagieren, dass in der Reaktionslösung weder der Titrator noch der Titrant im Überschuss vorliegt).
4. Bestimmt man nun das verbrauchte Volumen der genau bekannten Maßlösung, gelingt durch einfache Berechnungen die Bestimmung, z. B. der Konzentration des gesuchten Stoffes in der Analysenlösung.
Säure-Base-Titrationen (Neutralisationstitrationen)
Eines der genauesten und einfachsten maßanalytischen Titrationsverfahren ist die Säure-Base-Titration. Wie aus der Bezeichnung ersichtlich, werden eine Säure und eine Base bis zur vollständigen Neutralisation zur Reaktion gebracht. Aus dem Verbrauch an Maßlösung bis zum Äquivalenzpunkt berechnet man die Konzentrationen von Säure- bzw. Base in der Analysenlösung.
Dabei wird ausgenutzt, dass die Wasserstoff-Ionen (Hydronium-Ionen) der Säurelösung mit den Hydroxid-Ionen der Baselösung zu Wassermolekülen reagieren und sich entsprechend der pH-Wert der Lösung ändert. Am Äquivalenzpunkt sind die Mengen der Säure und der Base exakt gleich.
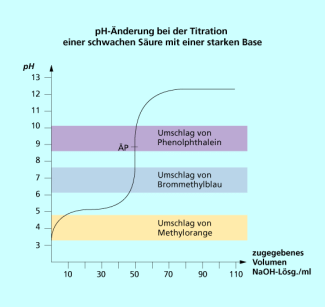
Zur Bestimmung des Äquivalenzpunktes (ÄP) dienen häufig Säure-Basen-Indikatoren, die die Veränderung des pH-Wertes durch Farbänderung anzeigen. Der Farbumschlag des Indikators charakterisiert den Punkt, an dem die Stoffmenge der zugegebenen Hydroxid-Ionen der Stoffmenge der in der Analysenlösung vorhandenen Wasserstoff-Ionen (Hydronium-Ionen) entspricht.
-
Kallayanee Naloka - shutterstock
Stellt man den Verlauf einer Säure-Base-Titration grafisch dar, erhält man eine Titrationskurve. Auf der Ordinate trägt man den pH-Wert, auf der Abszisse den Verbrauch an Maßlösung ab. Mit elektronischen Messgeräten, wie einem pH-Meter kann die Veränderung des pH-Wertes gemessen und dann abgetragen werden (Bild 2).
Betrachtet man die Kurve mathematisch, dann lässt sich ein Wendepunkt der Funktion berechnen. Dieser entspricht dem oben genannten Äquivalenzpunkt, an dem die Stoffmenge der zugegebenen Maßlösung gleich der Stoffmenge der unbekannten Analysenlösung ist.
Der Verlauf einer solchen Titrationskurve hängt stark von den beteiligten Säuren und Basen ab. Die bei der Titration ermittelten Werte werden als Grundlage der Berechung genutzt.
Beispiel:
Soll zum Beispiel der Säuregehalt eines aus der Schwefelsäureproduktion stammenden Abwassers im Labor geprüft werden, titriert man im Allgemeinen mit einer Natriumhydroxidlösung bekannter Konzentration.
Bei einer Routinetitration wurden für die Neutralisation von 20 ml entnommenem schwefelsäurehaltigen Abwasser 5 ml Natronlauge verbraucht.
Es kann der Indikator Bromthymolblau verwendet werden. (Der pH-Wert der bei der Neutralisation gebildeten Salzlösung sollte in der Mitte des Umschlagbereiches des Indikators liegen.)
Zur Auswertung von Titrationen betrachtet man die Neutralisationsgleichung der Titration:
Geht man von einer vollständigen Umsetzung der beiden Reaktionsteilnehmer aus, ergibt sich ein Stoffmengenverhältnis
Die Stoffmengen ergeben sich aus dem Produkt von verbrauchtem Volumen und Konzentration .
Nach diesem Prinzip lässt sich die Konzentration jeder beliebigen in Wasser löslichen Säure auf der Grundlage der entsprechenden Neutralisationsgleichung berechnen.
Der Äquivalenzpunkt bei Säure-Base-Titrationen lässt sich nicht nur mithilfe von Farbindikatoren ermitteln. Auch mit dem pH-Meter lässt sich die Änderung des pH-Werts der Analysenlösung messen und aus der Titrationskurve der Äquivalenzpunkt berechnen. Dazu nutzt man eine spezielle Elektrode, deren Spannung bzw. Elektrodenpotenzial nur vom pH-Wert der Lösung abhängt. Deshalb spricht man auch von potenziometrischer Titration.
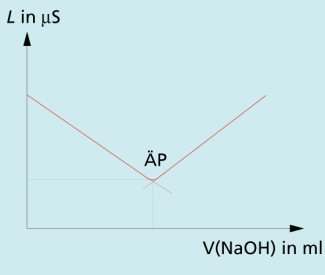
Eine andere Möglichkeit besteht darin, die Änderung der elektrischen Leitfähigkeit der Lösung während der Titration zu messen. Da bei der Neutralisation aus elektrisch geladenen Wasserstoff- und Hydroxid-Ionen elektrisch neutrale Wassermoleküle gebildet werden, ändert sich die Leitfähigkeit der Lösung im Laufe der Titration und erreicht am Äquivalenzpunkt ein Minimum (Bild 3)Aus dem Volumen an Maßlösung, das bis zu diesem Minimum verbraucht wurde lässt sich wieder die Konzentration der Analysenlösung berechnen. Diese Methode wird als konduktometrische Titration bezeichnet.
Die Nutzung elektronischer Messgeräte bietet die Möglichkeit, Titrationen nicht manuell sondern halbautomatisch oder sogar vollautomatisch durchzuführen. Die Darstellung der elektronisch erfassten Messwerte als Grafik kann sowohl mithilfe eines Computers als auch mithilfe eines grafikfähigen Taschenrechners mit geeigneter Zusatzsoft- und -hardware erfolgen.
In modernen Labors genutzte Titrierautomaten pumpen die Maßlösung wohldosiert über elektronische Büretten in die Analysenlösung. Die Änderung der Spannung (Potenzial) oder der Leitfähigkeit der Lösung wird ebenfalls elektronisch gemessen und ausgewertet. Die Software erstellt aus den Werten die Titrationskurve, ermittelt den Äquivalenzpunkt und berechnet die Konzentration der Probenlösung. Da bei dieser automatischen Titration die meisten menschlichen Fehler ausgeschlossen werden, sind die automatisierten Verfahren noch genauer und zuverlässiger als die gute alte manuelle Titration.
Das einfache und zuverlässige Grundprinzip der titrimetrischen Maßanalyse lässt sich auch auf andere Reaktionstypen übertragen. Nach der Art der ablaufenden Reaktionen unterscheidet man mehrere Arten von Titrationen. Die im Folgenden kurz genannten Methoden sind für viele verschiedene analytische Zwecke nutzbar (Bild 4).
Bei Redoxtitrationen wird mithilfe von Maßlösungen geeigneter Oxidationsmittel der Gehalt an reduzierend wirkenden Stoffen in einer Analysenlösung bestimmt. Umgekehrt kann auch ein Reduktionsmittel zu Bestimmung oxidierend wirkender Stoffe eingesetzt werden. Auf diese Weise ermittelt man beispielsweise den Sauerstoffgehalt in Wasserproben. Der Sauerstoffgehalt ist ein wichtiger Parameter für die Gewässergüte, der u. a. anzeigt wie gut die Lebensbedingungen für Wasserorganismen sind.
Bei Fällungstitrationen bilden Titrant und Titrator einen schwer löslichen Niederschlag. Wenn der Titrant vollständig verbraucht ist, steigt die Konzentration des Titrators bei weiterer Zugabe der Maßlösung an. Die Konzentrionsänderung wird in der Regel potenziometrisch verfolgt und auf diese Weise der Äquivalenzpunkt bestimmt. Beispielsweise kann der Gehalt an Chlorid-Ionen mit einer Silbernitratlösung bestimmt werden. Bei diesem Beispiel fällt Silberchlorid (AgCl) als schwer löslicher Niederschlag aus.
Eine vierte Variante der titrimetrischen Maßanalyse ist die komplexometrische Titration. Diese Methode dient hauptsächlich zur Bestimmung Konzentration mehrwertiger Metall-Ionen in wässrigen Lösungen. Sie beruht auf der Ausbildung besonderer Verbindungen – den Komplexverbindungen. Auch diese Methoden kommen bei der Wasseranalyse zum Einsatz. Mit ihrer Hilfe kann z. B. die so genannte Wasserhärte (der Gehalt an Calcium- und Magnesium-Ionen) quantitativ sehr genau bestimmt werden.
Titrationen sind allerdings zeitaufwendig. Für Routineuntersuchungen hat man durch Messung einer konzentrationsproportionalen physikalischen Größe oft sofort den Gehalt des gesuchten Stoffs. Durch Messung der Leitfähigkeit erhält man sofort den Gehalt an Schwefelsäure im Abwasser, und die Konzentration an Schwefelsäure in einem Bleiakkumulator kann man schnell durch eine Messung der Dichte ermitteln.
-

Heinz Mahler, Berlin