Störfaktoren der Embryonalentwicklung
Der Embryo ist während seiner Entwicklung normalerweise gut geschützt. Dennoch gibt es verschiedene Störfaktoren, die zu Fehlentwicklungen, schweren Missbildungen des Embryos oder zum Abort führen können.
Zu diesen schädigenden Einflüssen gehören genetische und mütterliche Faktoren sowie Umweltfaktoren wie Medikamente, Chemikalien, Suchtmittel, Strahlung und Infektionserreger, die spezifische Entwicklungsstörungen hervorrufen. Die Anfälligkeit für solche Störfaktoren sowie das Ausmaß der ausgeprägten Missbildungen sind wesentlich von dem Zeitpunkt der Einwirkung abhängig.
Während der sensiblen Phase, in der komplexe und grundlegende Prozesse der Organogenese ablaufen, wirken solche Störfaktoren besonders fatal.
Die Embryonalentwicklung ist ein komplexer Vorgang mit fein aufeinander abgestimmter Koordination der Zellteilung und -determinierung. Die Versorgung des Embryos mit Nährstoffen und Gasen, die für die Entwicklung erforderlich sind, erfolgt bei Säugetieren über die Plazentamembran durch den Austausch mit dem Blut der Mutter.
Die bis in die 30er-Jahre vorherrschende Meinung, der sich entwickelnde Embryo sei weitgehend vor äußeren schädigenden Einflüssen geschützt, wurde spätestens seit der Rötelepidemie 1941 neu überdacht, als der australische Arzt NORMAN McALISTER GREGG (1892-1966) den ursächlichen Zusammenhang zwischen den Fehlbildungen der Embryos und der Infektion der Mutter während der Schwangerschaft erkannte. Aus dieser Einsicht entwickelte sich eine neue Perspektive der Embryologie, indem bei auffälligen Fehlentwicklungen Ursachenforschung betrieben wurde und im Folgenden Störfaktoren der Embryonalentwicklung ermittelt werden konnten.
Heute ist bekannt, dass vielfältige embryonale, mütterliche und umweltbedingte Faktoren die fetale Wachstumsrate beeinflussen bzw. zu Fehlentwicklungen des entstehenden Lebens führen können. Dabei weist der Embryo in den verschiedenen Phasen der Embryonalentwicklung eine unterschiedliche Sensibilität für spezifische Störfaktoren auf. Während der ersten Woche nach der Befruchtung bis zur Einnistung der Blastula in der Uteruswand gilt bei Störeinwirkung das „Alles-oder-Nichts-Prinzip“, das heißt es kommt entweder zum Abort oder zur Regeneration.
Generell können Störfaktoren beim Menschen während der ersten 10 Schwangerschaftswochen besonders schwere Fehlentwicklungen hervorrufen, da in dieser Phase die grundlegenden Prozesse der Musterbildung (Morphogenese) und Differenzierung determinierter Zellen (Histogenese) ablaufen, die zur Bildung der Organe führen. Daher wird dieser Zeitraum als kritische oder sensible Phase der Embryonalentwicklung bezeichnet, wobei jedem Organ eine eigene sensible Phase zugeordnet werden kann. In der darauffolgenden Fetalperiode, die durch Wachstum, Differenzierung und Funktionsentwicklung der Organe charakterisiert ist, nimmt die Sensibilität für Störfaktoren ab.
Die Fehlbildungsrate beim Menschen zum Zeitpunkt der Geburt beträgt in Deutschland etwa 4-8 % und stellt die zweithäufigste Ursache der Säuglingssterblichkeit dar.
Mütterliche Faktoren
Zu den mütterlichen Faktoren, die in dieser Statistik eine Rolle spielen, zählen z. B. Stoffwechselerkrankungen (Phenylketonurie, Diabetes mellitus) oder Mangelernährung während der Schwangerschaft.
-
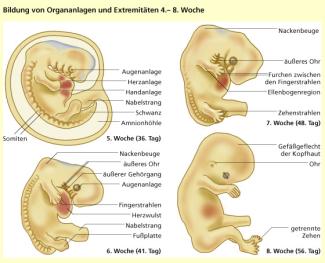
Embryonalentwicklung des Menschen: Bildung von Organanlagen und Extremitäten
Genetische Faktoren
Genetische Faktoren zählen mit Anteilen von mehr als einem Drittel zu den prozentual relevantesten Faktoren, die zu Störungen der Embryonalentwicklung führen können.
Dazu gehören Genmutationen und Chromosomenanomalien.
Genmutationen können Veränderungen oder Verluste von Genfunktionen auslösen, die beim Embryo Fehlentwicklungen hervorrufen. Mutationen in Entwicklungsgenen führen zu gestörter Musterbildung, das Gewebe selbst ist jedoch histologisch normal. Ein Beispiel ist die Polydaktylie (Mehrfingrigkeit), bei der zusätzliche Finger oder Zehen ausgebildet werden. Missbildungen, die auf Genmutation beruhen, werden nach den mendelschen Regeln weitervererbt.
Chromosomenanomalien zählen mit etwa 61 % zu den häufigsten Ursachen von Aborten vor der 20. Woche. Bei der numerischen Chromosomenanomalie erfolgt in den meisten Fällen die Trennung während der ersten oder zweiten meiotischen Teilung nicht vollständig. Die wohl bekannteste Anomalie dieser Kategorie ist die Trisomie 21 (Down-Syndrom), bei der das Chromosom 21 dreimal in der Zygote enthalten ist statt wie bei der normalen Entwicklung doppelt. Diese Anomalie führt zu einer charakteristischen phänotypischen Ausprägung.
Strukturelle Chromosomenanomalien basieren meist auf Chromosomenbrüchen, durch die es zu Verdoppelung oder Verlust von Chromosomensegmenten kommen kann. Ursachen für strukturelle Aberrationen können durch genetische Dispositionen der Eltern gegeben sein, bei denen Verlagerungen von Chromosomenabschnitten (Translokation) oder nach Brüchen umgekehrt eingefügte Chromosomensegmente (Inversion) zu einer Fehlbildung des Kinds führen.
Teratogene
Umwelteinflüsse wie radioaktive Strahlung oder krebserregend wirkende Chemikalien oder Viren gelten als wichtige Faktoren, die die Rate genetischer Mutationen oder struktureller Chromosomenanomalien steigern können. Solche Faktoren gehören zur Klasse der Teratogene. Teratogene werden als Faktoren oder Stoffe definiert, die zu Fehlbildungen beim Embryo führen oder deren Risiko erhöhen. Sie werden in folgende Kategorien eingeteilt:
Ionisierende Strahlung
Als „ionisierende Strahlen“ bezeichnet man hochfrequente elektromagnetische Wellen wie Röntgenstrahlen (γ-Strahlen) und kosmische Strahlung sowie α- und ß-Strahlung aus radioaktivem Zerfall. Sie wird auch bei der Krebstherapie eingesetzt, da sich ihre zellzerstörende Wirkung insbesondere auf sich schnell teilende Zellen wie Tumorzellen auswirkt. Daher ist eine Strahlenexposition für den Embryo besonders während der frühen Entwicklungsphase kritisch und kann zu Zelltod, Chromosomenveränderungen, Missbildungen und Wachstumsstörungen führen. Bei Schwangerschaften während der Atombombenexplosion von Hiroshima und Nagasaki 1945 waren fast ein Drittel Fehlgeburten zu verzeichnen, etwa ein Viertel der Neugeborenen starb im ersten Lebensjahr. Ein sehr hoher Prozentsatz der überlebenden Kinder wies verschiedenste Missbildungen auf, wobei häufig vor allem das zentrale Nervensystem (ZNS) betroffen war. Ähnliche Auswirkungen waren auch bei der Reaktorkatastrophe von Tschernobyl 1986 zu beobachten.
Radio- und Mikrowellen
Radio- und Mikrowellen gehören zu den elektromagnetischen Wellen, denen wir z. B. durch Mobilfunk in wachsendem Maße ausgesetzt sind. Bei Überschreitung bestimmter Schwellenwerte können unter ihrem Einfluss biologische Wirkungen aufgrund von Wärmeentwicklung auftreten. In Tierexperimenten wurde nachgewiesen, dass unter solchen Bedingungen Störungen der Embryonalentwicklung vorkommen können.
Infektionserreger
Röteln, eine Virusinfektion, führt bei Erkrankung der Mutter während der ersten Monate der Schwangerschaft mit einem hohen Prozentsatz zu Missbildungen beim Embryo. Dabei gilt, dass die Wahrscheinlichkeit einer Störung der Embryonalentwicklung steigt, je früher die Infektion erfolgt. So wird das Risiko in den ersten vier Wochen auf etwa 50 % geschätzt, während es im zweiten Monat auf 20 % sinkt und im dritten Monat noch bei etwa 6 % liegt.
Die durch die Erkrankung hervorgerufenen Fehlentwicklungen betreffen je nach Zeitpunkt und Verlauf der Infektion mit unterschiedlichem Schweregrad Herz, Innenohr oder Augen des Embryos. In Deutschland gibt es für Mädchen vor der Pubertät ein Impfprogramm gegen Röteln.
Bei Infektionen mit dem Zytomegalie-Virus während der ersten drei Schwangerschaftsmonate kommt es zu so gravierenden Schädigungen des Embryos, dass sie meist mit einem Abort einhergehen. Während der folgenden Fetalphase kann das Virus Missbildungen des Gehirns und der Augen oder Lähmungen verursachen.
Toxoplasmose wird durch einen intrazellulären, einzelligen Parasiten verursacht, der durch rohes oder wenig gekochtes Fleisch bzw. über den Kontakt mit Haustieren übertragen wird. Toxoplasmen können ungehindert die Plazentamembran passieren und den Fetus infizieren. Dies kann Veränderungen des Gehirns und Augenschäden beim Fetus zur Folge haben.
AIDS (human immunodefiency virus, HIV)
Gegen die Immunschwäche AIDS gibt es bislang noch keine ausreichende Therapie und die Zahl der mit HIV Infizierten im fortpflanzungsfähigen Alter nimmt ständig zu. Der Retrovirus HIV kann auch die Plazentaschranke durchdringen und den Fetus infizieren. In Abhängigkeit des Schwangerschaftsstadiums können beim Fetus unterschiedliche Störungen auftreten, wie z. B. Gesichtsfehlentwicklungen, Mikrozephalie, Wachstumsstörungen.
Medikamente/Chemikalien
Contergan®, ein Schlaf- und Beruhigungsmittel mit dem Wirkstoff Thalidomid, gehört sicher zu den bekanntesten teratogen wirkenden Medikamenten. Nach der Markteinführung von Contergan®, 1958, traten vor allem Extremitätenfehlbildungen aber auch Ohr-, Herz- Augen- und Gesichtsschädigungen sowie Anomalien des Verdauungstrakts bei Neugeborenen auf, deren Zahl auf etwa 7 000 Betroffene geschätzt wird. 1961 wurde es aus dem Handel genommen. Thalidomid wirkte ausschließlich bei Einnahme in frühen Schwangerschaftsstadien schädigend auf die Entwicklung des Embryos.
Antibiotika wie Tetracycline sind in der Lage, die Plazentamembran zu passieren und sich in Knochen und Zähnen des Embryos einzulagern. Dies kann Zahndefekte, Verfärbungen der Milchzähne sowie Störungen der Knochenentwicklung hervorrufen. Die Einnahme von Streptomycin und seinen Derivaten während der Fetalperiode birgt die Gefahr einer Hörstörung und Schädigung des 8. Hirnnerven (Hör- und Gleichgewichtsnerv) beim Fetus. Bei Hormonen lassen sich teratogene Wirkungen von männlichen Sexualhormonen nachweisen. Diese erhöhen beim weiblichen Fetus deutlich das Risiko einer Störung der Geschlechtsentwicklung und können zur Vermännlichung führen. Das männliche Sexualhormon Testosteron ist z. B. in Anabolika enthalten.
Medikamente zur Tumorbekämpfung (mutagene Pharmaka) wirken hochgradig teratogen, da sie die Zellteilungsaktivität hemmen. Dadurch kann es während der Einnahme in der Schwangerschaft in erhöhtem Maße zu Aborten und zu genetischen Schädigungen des Embryos kommen, die verschiedenartige schwere Missbildungen hervorrufen.
Suchtmittel
Bei übermäßigem Genuss von Alkohol während der Schwangerschaft können schwere körperliche und geistige Entwicklungs- und Wachstumsstörungen des Kinds auftreten. Die entsprechenden Symptome zusammenfassend spricht man von einer sogenannten Alkoholembryopathie, die sich im Detail u. a. in einer abnormen Kleinheit des Kopfs (Mikrozephalie), Herzfehlern, Nierenstörungen, Neuralrohrdefekten und Gelenkanomalien manifestiert. Auch bei mäßigem Alkoholkonsum können sich einige dieser Symptome ausprägen. Leichter betroffene Kinder können unter Lern- und Verhaltensstörungen leiden.
Nicotinkonsum hat zwar keine Missbildungen des Embryos zur Folge, kann jedoch das Wachstum des Fetus verzögern. Bei starken Raucherinnen entwickeln sich die Feten während der letzten 6-8 Wochen erwiesenermaßen langsamer. Da Nicotin die Gefäße verengt, kann dies zu einer Verminderung der Plazentadurchblutung und somit zu einer Sauerstoffunterversorgung führen, die in Folge das Zellwachstum negativ beeinflusst. Auch kann es zu Früh- oder Fehlgeburten kommen. Man schätzt, dass dieses Risiko bei mehr als 20 Zigaretten täglich etwa doppelt so hoch ist wie bei Nichtraucherinnen.
Weiterhin stehen auch Suchtmittel wie LSD, Kokain und Heroin in Verdacht, die Embryonalentwicklung massiv zu beeinträchtigen.
Die Anfälligkeit für Störfaktoren sowie die Art und Schwere ihrer Auswirkungen auf die Embryonalentwicklung zeigen sich in hohem Maße abhängig von:
- der Dosis des einwirkenden Faktors (Dosis-Wirkungsbeziehung),
- der genetischen Disposition der Embryonen,
- der genetischen Disposition der Mutter, da die genetische Konstitution der Mutter ein wichtiges Kriterium für die Stoffwechselumsetzung ist und teratogene Stoffe z. B. die Entwicklung des Embryos häufig nicht direkt, sondern über ihre Metabolite (Stoffwechselzwischenprodukte) stören,
- dem Zeitpunkt der Einwirkung des Störfaktors.
Bei der zunehmenden Zahl an Umweltchemikalien (z. B. auch Wohnraumgiften, Lebensmittelzusätzen, Pestiziden) ist die Vermeidung teratogener Einflüsse in der heutigen Zeit nicht einfach, da die Effekte vieler Stoffe auf die Embryonalentwicklung bislang noch unerkannt sein dürften. Zahlreiche Substanzen stehen wie Dioxin bereits unter Verdacht einer schädigenden Wirkung. Häufig jedoch lassen sich Störfaktoren der Embryonalentwicklung schon aufgrund der komplexen Abläufe und vielfältigen Einflüsse nicht eindeutig bestimmen oder nachweisen (in etwa 55 % der Fälle). Erst mit zunehmendem Wissen über die Funktionen von Genen, der Ermittlung von genetischen Mutationen und ihren Ursachen sowie der intensiven Kenntnis von Entwicklungsabläufen in Kombination mit einem Fehlbildungsmonitoring können weitergehende Erkenntnisse gewonnen werden, um den Schutz des werdenden Lebens vor gefährdenden Umwelteinflüssen weiter zu verbessern.
Suche nach passenden Schlagwörtern
- LSD
- radioaktiv
- Befruchtung
- Entwicklungsphase
- Teratogene
- Fehlbildungsmonitoring
- Stoffwechselerkrankung
- Hormone
- Medikamente
- Chromosomenaberration
- Umwelteinflüsse
- Chromosomensegmente
- Sensibilität
- Vererbung
- Geburt
- Metabolite
- Chromosomen
- Chromosomenbrüche
- Organe
- Präimplantationsphase
- Toxoplasmose
- Morphogenese
- Viren
- Röntgenstrahlung
- Zelltod
- Stoffwechsel
- Wirkstoffe
- Fetus
- Rauchen
- Umweltfaktoren
- Trisomie
- infizieren
- Chromosomenanomalien
- genetische Faktoren
- Virus
- Einflüsse
- Zellteilung
- Organanlagen
- Kokain
- Contergan
- Anabolika
- elektromagnetische Felder
- Wachstumsstörung
- umweltbedingt
- Störungen
- mütterliche Faktoren
- Höhenstrahlung
- Zytomegalie-Virus
- Erkrankung
- Infekt
- Risiko
- Plazentamembran
- Umweltchemikalien
- Uterus
- Chromosomenabschnitte
- Embryonalentwicklung
- Histogenese
- Thalidomid
- Fetalphase
- Infektion
- Embryologie
- Radiowellen
- fetal
- Embryonalphase
- Suchtmittel
- Wachstumsrate
- embryonal
- Störfaktoren
- Translokation
- Wachstum
- Wirkung
- Blastula
- Schwangerschaft
- Alkoholembryopathie
- Zigaretten
- strukturelle Chromosomenanomalie
- Schädigung
- Chemikalien
- Strahlung
- Abort
- Mutagen
- Antibiotika
- Infektionserreger
- Aids
- Virusinfektion
- Down-Syndrom
- ionisierende Strahlung
- Fehlbildungsrate
- Radioaktivität
- Testosteron
- mendelsche Regel
- Inversion
- Trisomie 21
- Genfunktion
- Genmutation
- Entwicklung
- Anomalie
- numerische Chromosomenanomalien
- Kritische Phase
- HIV
- Schwangerschaftsstadium
- Heroin
- Embryo
- Alkohol
- Neugeborene
- Sexualhormon
- Mutter
- Missbildung
- Entwicklungsgene
- Gene
- Fehlbildung
- Fehlentwicklung
- Umwelt
- Sensible Phase
- Röteln
- Dioxin
- Nikotin

